
| A. | 石油主要含碳、氢元素,是烷烃、环烷烃、芳香烃的混合物 | |
| B. | 石油中含有C5~C11的烷烃,可以通过石油的常压分馏得到汽油 | |
| C. | 含C20以上烷烃的重油经减压分馏可以得到煤油和柴油 | |
| D. | 石油经分馏得到的各馏分仍是多种烃的混合物 |
分析 A、石油是多种烷烃和环烷烃的混合物,还含有少量的芳香烃;
B、汽油经石油的常压分馏得到;
C、煤油和柴油是石油的常压分馏产物;
D、石油的馏分仍然是混合物.
解答 解:A、石油是多种烷烃和环烷烃的混合物,还可能含少量的芳香烃,故A正确;
B、汽油经石油的常压分馏得到,是碳原子数在C5~C11的烷烃的混合物,故B正确;
C、煤油和柴油是石油的常压分馏产物,含C20以上烷烃的重油经减压分馏可以得到润滑油、石蜡油等,故C错误;
D、石油的馏分仍然是混合物,没有固定的熔沸点,故D正确.
故选C.
点评 本题考查了石油的综合利用,难度不大,应注意的是石油中含有芳香烃,常压分馏得到汽油、煤油、柴油等轻质油,减压分馏得到沥青、石蜡油和润滑油等.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:实验题
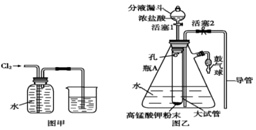 氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).
氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).查看答案和解析>>
科目:高中化学 来源: 题型:实验题
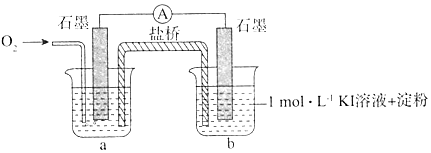
| 装置 | 烧杯中的液体 | 现象(5分钟后) |
 | ①2mL1mol/LKl溶液+5滴淀粉 | 无明显变化 |
| ②2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L HCl | 溶液变蓝 | |
| ③2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L KCl | 无明显变化 | |
| ④2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
| 烧杯中的液体 | 现象(5小时后) |
| ⑤2mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀粉 | 溶液才略变蓝 |
| ⑥2mLpH=10混有KOH的1mol/L KI溶液+5滴淀粉 | 无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素在人体内具有抗氧化、增强免疫力等功效 | |
| B. | 元素符号为 Sn | |
| C. | 在元素周期表中位于第四周期第ⅣA 族 | |
| D. | 属于金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式为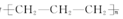 | B. | 丙烷分子的比例模型为 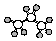 | ||
| C. | 四氯化碳分子的电子式为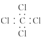 | D. | 2-乙基-1,3-丁二烯的键线式: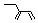 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 奶精能使溴水和酸性KMnO4溶液褪色,其原理相同 | |
| B. | 氢化植物油在稀H2SO4和NaOH溶液中发生水解,所得产物相同 | |
| C. | 白砂糖在人体内水解转化为果糖而被人体吸收 | |
| D. | 奶粉可作为人体所需的一种营养物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石比石墨稳定 | B. | 石墨转化为金刚石需要吸热 | ||
| C. | 金刚石燃烧产物更稳定 | D. | 等质量时,石墨所含能量高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com