

 ,随意丢弃聚氯乙烯制品会造成白色污染.
,随意丢弃聚氯乙烯制品会造成白色污染.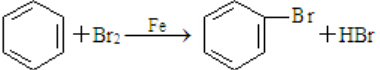 ,该反应中反应物溴应该选用液溴(填“溴水”或“液溴”).
,该反应中反应物溴应该选用液溴(填“溴水”或“液溴”).分析 (1)乙烯和水在催化剂、加热、加压条件下发生加成反应生成A为CH3CH2OH,A在浓硫酸作催化剂、加热条件下发生反应生成C,C具有水果香味,说明C中含有酯基,则B为羧酸,C为酯,
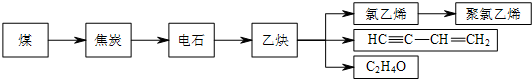
①以石油为原料的系列化工生产过程中,得到大量乙烯的主要方法是裂解;
②有机物A俗称酒精,乙醇中官能团为醇羟基,在170℃、浓硫酸作催化剂条件下,能用乙醇制取乙烯;
③B的分子式为C2H4O2,与纯碱反应能生成二氧化碳气体,说明含有羧基,其结构简式为CH3COOH;
(2)①电石和水反应生成氢氧化钙和乙炔,氯乙烯发生加聚反应生成聚氯乙烯;随意丢弃聚氯乙烯制品会造成 白色污染;
分别完全燃烧等质量的HC≡C-CH=CH2和乙炔,二者的最简式相同,其耗氧量与有机物的质量成正比;
醛能发生银镜反应,也能和新制氢氧化铜悬浊液反应生成砖红色沉淀;
②在溴化铁作催化剂条件下,苯和液溴发生取代反应生成溴苯;
③焦炉气具有可燃性,其主要成分是H2和甲烷.
解答 解:(1)乙烯和水在催化剂、加热、加压条件下发生加成反应生成A为CH3CH2OH,A在浓硫酸作催化剂、加热条件下发生反应生成C,C具有水果香味,说明C中含有酯基,则B为羧酸,C为酯,
①以石油为原料的系列化工生产过程中,得到大量乙烯的主要方法是裂解,故选c;
②有机物A俗称酒精,乙醇中官能团为醇羟基,在170℃、浓硫酸作催化剂条件下,乙醇发生消去反应生成乙烯,故答案为:酒精;醇羟基;170;
③B的分子式为C2H4O2,与纯碱反应能生成二氧化碳气体,说明含有羧基,其结构简式为CH3COOH,乙醇和乙酸酯化反应方程式为CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,为取代反应或酯化反应,
故答案为:CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;取代反应或酯化反应;
(2)①电石和水反应生成氢氧化钙和乙炔,反应方程式为CaC2+2H2O→Ca(OH)2+C2H2↑;氯乙烯发生加聚反应生成聚氯乙烯,聚氯乙烯结构简式为 ,随意丢弃聚氯乙烯制品会造成 白色污染;
,随意丢弃聚氯乙烯制品会造成 白色污染;
分别完全燃烧等质量的HC≡C-CH=CH2和乙炔,二者的最简式相同,其耗氧量与有机物的质量成正比,二者质量相等,所以耗氧量一样多;
醛能发生银镜反应,也能和新制氢氧化铜悬浊液反应生成砖红色沉淀,所以常用银氨溶液或新制氢氧化铜悬浊液来检验醛基;
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑; ;一样多;银氨溶液或新制氢氧化铜悬浊液;
;一样多;银氨溶液或新制氢氧化铜悬浊液;
②在溴化铁作催化剂条件下,苯和液溴发生取代反应生成溴苯,反应方程式为 ,
,
故答案为: ;液溴;
;液溴;
③焦炉气具有可燃性,其主要成分是H2和另一种气体,该气体是最简单的烃,为CH4,故答案为:CH4.
点评 本题考查有机物推断及合成,为高频考点,侧重考查学生分析推断及知识综合运用能力,明确物质之间的转化、反应条件及物质性质是解本题关键,注意:苯和溴水不反应,和液溴在催化剂条件下发生取代反应.


科目:高中化学 来源: 题型:选择题
| A. | 原子晶体 | B. | 分子晶体 | C. | 离子晶体 | D. | 金属晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 摩尔任何物质都含NA个原子 | |
| B. | 0.1 mol/L K2SO4溶液中含有 K+为0.2 NA | |
| C. | 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数一定为0.2NA | |
| D. | 标准状况下,22.4L 以任意比混合的CO、CO2混合气体所含碳原子数约为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的乙酸、葡萄糖与淀粉完全燃烧时消耗氧气的质量相等 | |
| B. | 按系统命名法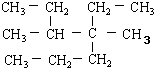 的名称为4,5-二甲基-4-乙基庚烷 的名称为4,5-二甲基-4-乙基庚烷 | |
| C. | 豆浆中富含大豆蛋白,煮沸后蛋白质水解成了氨基酸 | |
| D. | 某烯烃(最简式为CH2)与H2加成产物为2,3-二甲基丁烷,则该烯烃可能有2种结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
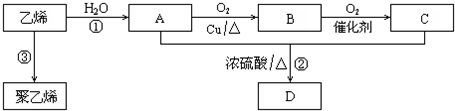
 ;反应类型:加聚反应
;反应类型:加聚反应查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上制取氯酸钾的主要步骤为:
工业上制取氯酸钾的主要步骤为: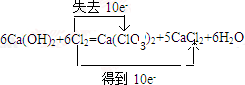 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com