
分析 混合气体的物质的量为$\frac{4.48L}{22.4L/mol}$=0.2mol,n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(CO2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,烯烃通式为CnH2n,可根据生成二氧化碳和水的量列式计算,以此解答该题.
解答 解:设CO xmol、CnH2n ymol,
混合气体:$\frac{4.48L}{22.4L/mol}$=0.2mol,
n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol n(H)=0.6mol,
n(CO2)=$\frac{8.96L}{22.4L/mol}$=0.4mol n(C)=0.4mol,
则x+y=0.2,x+ny=0.4,2ny=0.6,
x=0.1mol,
y=0.1mol,
n=3,
所以烯烃分子式为C3H6,结构简式为CH3CH=CH2.
答:该烯烃的结构简式为CH3CH=CH2.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,熟练掌握常见有机物结构与性质为解答关键,注意掌握质量守恒定律在确定有机物分子式中的应用方法.


科目:高中化学 来源: 题型:解答题
| 可能与某类物质反应 | 具体的离子反应方程式 | |
| CuCl2 | 金属单质 | ①Cu2++Fe=Cu+Fe2+ |
| ②氢氧化钠 | ③Cu2++2OH-=Cu(OH)2↓ | |
| ④硝酸银 | Ag++Cl-═AgCl↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24LC2H4和C2H2的混合气体中含碳原子数目小于0.2NA | |
| B. | 100mL1.0mol/L的FeCl3溶液与足量Cu反应,转移电子数数为0.2NA | |
| C. | 标况下44.8mL氯气通入足量水中发生反应,转移电子数为2×10-3NA | |
| D. | 常温下,pH=2的H2SO4溶液中含有的H+数目为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
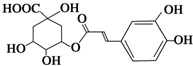 从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )
从金银花中提取的绿原酸结构简式如图所示.其有抗菌、消炎、解毒.利胆.降压和增加胃肠蠕动的作用.用于急性细菌性感染及放、化疗所致的白细胞减少症.下列说法不正确的是( )| A. | 绿原酸的分子式为C16H18O9 | |
| B. | 绿原酸及其水解产物之一在空气中均能稳定存在,遇FeCl3溶液时显紫色 | |
| C. | 1mol绿原酸与NaOH溶液反应时,最多消4molNaOH | |
| D. | 1mol绿原酸与足量金属Na反应时能产生3molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 天然物质都是绿色无毒的物质 | B. | 只饮用纯净水有益人体健康 | ||
| C. | 禁止吸烟可减少室内空气污染 | D. | 微量元素只能通过保健品摄入 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c (NH3•H2O)>c (NH4+)>c (H+)>c (OH-) | B. | c (NH4+)>c (NH3•H2O)>c (OH-)>c (H+) | ||
| C. | c (NH3•H2O)>c (NH4+)=c (OH-)>c (H+) | D. | c (NH3•H2O)>c (OH-)>c (NH4+)>c (H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2、Al(OH)3 | B. | Al(OH)3、NaHCO3 | C. | Na2SO3、Mg(OH)2 | D. | Na2CO3、CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图中新月形分子和环状分子“组合”在一起,铜离子起关键作用 | |
| B. | 利用此方式可以合成新分子,同时也可能创造一种全新“机械键” | |
| C. | 在创造新分子技术中,铜离子是唯一可以借助的金属离子 | |
| D. | 此技术可以“互锁”合成  分子,甚至成更复杂的分子 分子,甚至成更复杂的分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com