
| A、密度:K>Na |
| B、离子半径:H->Li+ |
| C、碱性:LiOH>NaOH |
| D、熔沸点:Rb>K |


科目:高中化学 来源: 题型:
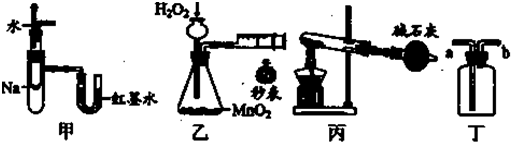
| A、装置甲可用于验证反应的热效应 |
| B、装置乙可定量测定化学反应的速率 |
| C、装置丙可用于实验室以NH4Cl为原料制备少量NH3 |
| D、装置丁a口进气可收集NH3、C12等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④ | B、①③⑤ |
| C、①②③ | D、①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.15 mol?L-1 |
| B、0.2 mol?L-1 |
| C、0.3 mol?L-1 |
| D、0.4 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不宜用瓷坩埚灼烧氢氧化钠或碳酸钠 |
| B、定容后,倒置容量瓶摇匀经平放静置,液面低于刻度线,再加水定容 |
| C、使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏大 |
| D、用铝箔包住部分被氧化成Na2O的钠块,并用镊子夹住在水槽中反应,用倒置的量筒量取生成气体的体积,可以计算钠块中钠单质的质量分数 |
| E、用托盘天平称量11.74g氯化钠晶体 |
| F、为了使稀硫酸和锌制取氢气的速率加快,可向稀硫酸中加入用铜网包裹的锌粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、皮肤上沾上浓硫酸应立即用氢氧化钠溶液中和 |
| B、酒精灯中酒精不慎洒出在桌上燃烧,应立即用湿布扑盖 |
| C、氢氧化钠溶液溅到眼睛中,立即闭上眼睛,轻轻揉搓 |
| D、实验中出现轻微气体中毒,受伤人员应立即伏到实验桌上好好休息 |
查看答案和解析>>
科目:高中化学 来源: 题型:
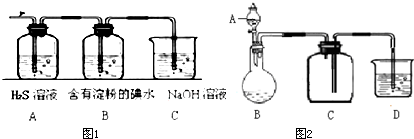
查看答案和解析>>
科目:高中化学 来源: 题型:
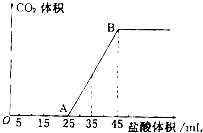 实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题
实验室欲配制0.1mol/L NaOH溶液并进行有关性质实验,请据此回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com