
向一定量Fe、FeO、Fe2O3的混合物中,加入50mL1mol·L-1硫酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的混合物,能得到铁的质量为
A. 11.2g B. 2.8g C. 5.62g D. 无法计算
科目:高中化学 来源:2016-2017学年江西省南昌市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组物质依次满足如图所示转化 关系的是(图中箭头表示一步转化) ( )
关系的是(图中箭头表示一步转化) ( )
a | b | c | d | |
① | Si | SiO2 | H2SiO3 |
|
② | Al | AlCl3 | NaAlO2 | Al(OH)3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Na | NaOH | Na2CO3 | NaHCO3 |
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省安庆市高一上学期期末考试化学试卷(解析版) 题型:简答题
—实验室有甲、乙两瓶无色溶液,标签已脱落,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液。为测定甲、乙两瓶溶液的成分及物质的量浓度,进行以下实验:
①取40mL甲溶液,向其中缓慢滴入乙溶液50mL,立即有气体产生并共收集到224mL(标准状况)气体。
②取50mL乙溶液,向其中缓慢滴入甲溶液40mL,开始没有气体,滴定一定的量后有气体产生,并共收集到112mL(标准状况)气体。
(1)判断:甲是____________溶液,乙是____________溶液;(均填化学式每空1分)
(2)实验中①所发生反应的离子方程式:______________________________;
(3)甲溶液的物质的量浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省安庆市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列反应既属于基本反应类型(化合、分解、置换、复分解),又属于氧化还原反应的是
A. 4Fe(OH)2+O2+2H2O=4Fe(OH)3 B. 2FeCl3+2KI===2FeCl2+2KCl+I2
C. 3CO+Fe2O3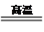 2Fe+3CO2 D. Si+2NaOH+H2O=Na2SiO3+2H2↑
2Fe+3CO2 D. Si+2NaOH+H2O=Na2SiO3+2H2↑
查看答案和解析>>
科目:高中化学 来源:湖南省长沙市2016-2017学年高一上学期期末考试化学试卷 题型:实验题
硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应,硼与氯气反应生成三氯化硼(BC13),生成的三氯化硼遇水水解产生白雾(已知:BC13的熔点为-107. 3℃,沸点为12.5 ℃),且三氯化硼用于制取乙硼烷(B2H6)。某兴趣小组设计如图所示装置制备三氯化硼。
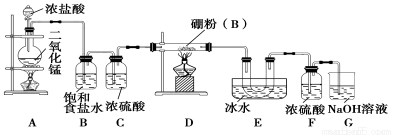
回答下列问题:
(1)装置D中发生反应的化学方程式为_____________________。
(2)装置B、E的作用分别是________________、________________。
(3)可以用盛装____________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
(4)为了顺利完成实验,点燃酒精灯的正确操作是______(填字母),其理由是__________。
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯
查看答案和解析>>
科目:高中化学 来源:湖南省长沙市2016-2017学年高一上学期期末考试化学试卷 题型:选择题
下列各组物质稀溶液相互反应。无论前者滴入后者,还是后者滴入前者,反应现象都相同的是
A. Na2CO3溶液与HCl溶液
B. AlCl3溶液与NaOH溶液
C. KAlO2 溶液与HCl溶液
D. Na2Si3溶液和HCl溶液
查看答案和解析>>
科目:高中化学 来源:湖南省长沙市2016-2017学年高一上学期期末考试化学试卷 题型:选择题
下列关于纯净物,混合物,强电解质,弱电解质和非电解质的正确组合是
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 纯盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
B | 冰醋酸 | 空气 | 硫酸钡 | 亚硫酸 | 二氧化硫 |
C | 氯气 | 盐酸 | 苛性钠 | 氢硫酸 | 碳酸钙 |
D | 漂白粉 | 氨水 | 氯化钠 | 次氯酸 | 氯气 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届云南省昆明市新课标高三月考卷(六)理综化学试卷(解析版) 题型:简答题
发展以煤制乙烯、丙烯、丁烯等低碳烯烃,部分替代石油化工产品的道路是我国保障能源安全战略的重要措施。间接法是先由煤制合成气(组成为H2、CO和少最的CO2)制备甲醇或二甲醚(CH3OCH3),其主要过程包括以下四个反应:
甲醇合成反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.1 kJ•mol-1
CH3OH(g) △H1=-90.1 kJ•mol-1
②CO2(g)+3H2(g) CH3OH(g) +H2O(g) △H2=-49.0kJ•mol-1
CH3OH(g) +H2O(g) △H2=-49.0kJ•mol-1
水煤气变换反应:
③CO(g)+ H2O(g) CO2(g)+ H2(g) △H3=-41.1kJ•mol-1
CO2(g)+ H2(g) △H3=-41.1kJ•mol-1
二甲醚合成反应:
④2CH3OH(g) CH3OCH3(g)+H2O(g) △H4=-24.5kJ•mol-1
CH3OCH3(g)+H2O(g) △H4=-24.5kJ•mol-1
回答下列问题:
(1)分析上述反应(均可逆),发生反应④对于CO转化率的影响是_______(填“增大”、“减小”或“无影响”,其理由是__________。
(2)在二个体积均为1.0L的恒容密闭容器中发生上述二甲醚合成反应④。实验数据见下表:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
b | 387 | 0.40 | 0 | 0 | ||
c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
①387℃时,反应④的化学平衡常数K=__________。
②达到平衡时,容器b中CH3OH的转化率为________。
③达到平衡时,容器c中CH3OCH3的体积分数为________。
(3)由H2和CO可直接制备二甲醚:2CO2(g)+4H2(g)=CH3OCH(g)+H2O(g) ΔH=__________;为提高反应物的转化率,根据化学反应原理,理论上应采取的措施是________(填序号)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
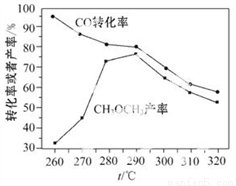
(4)有研究者用Cu-Zn-Al和Al2O3作催化剂,压强为5.0 MPa的条件下,由合成气[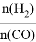 =2]直接制备二甲醚,结果如下图所示.已知:选择性=
=2]直接制备二甲醚,结果如下图所示.已知:选择性=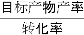 ×100%。则有图可知二甲醚的选择性达最大值时对应的温度是____________。
×100%。则有图可知二甲醚的选择性达最大值时对应的温度是____________。
(5)2016年,我国的两个科研团队在合成气直接制备低碳烯烃(nCO+2nH2 CnH2n+nH2O)的研究中连续取得重大突破,论文分别发表在《德国应用化学》(2016.03.16)、《Nature》(2016.10.06)杂志上。
CnH2n+nH2O)的研究中连续取得重大突破,论文分别发表在《德国应用化学》(2016.03.16)、《Nature》(2016.10.06)杂志上。 =2时,前者在400℃,1MPa的条件下,CO转化率为11%,低碳烯烃选择性达74%;后者在250℃,0.1~0.5MPa的条件下,CO转化率为31.8%,低碳烯烃选择性为60.8%,则其中低碳烯烃的产率较大者的值为_________。
=2时,前者在400℃,1MPa的条件下,CO转化率为11%,低碳烯烃选择性达74%;后者在250℃,0.1~0.5MPa的条件下,CO转化率为31.8%,低碳烯烃选择性为60.8%,则其中低碳烯烃的产率较大者的值为_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高二上学期期末考试化学试卷(解析版) 题型:选择题
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A. 原子核内有10个中子的氧原子:18O B. 乙烯的结构简式: CH2CH2
C. CH4分子的比例模型: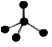 D. -CH3(甲基)的电子式为:
D. -CH3(甲基)的电子式为: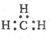
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com