
汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。
Ⅰ.CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1= —574 kJ·mol- 1 .
CH4(g) + 4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2= 一1160 kJ·mol- 1
(1)甲烷直接将NO2还原为N2的热化学方程式为 ;
Ⅱ.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
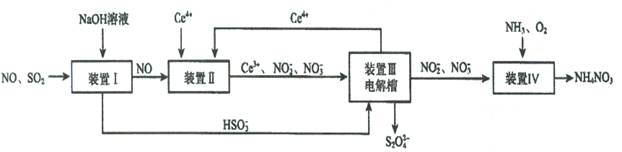
(2)装置Ⅱ中,酸性条件下,NO被Ce 4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO3- 的离子方程式 ;
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
①生成的Ce4+ 从电解槽的 (填字母序号)口流出;
②生成S2O42 - 的电极反应式为 ;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g·L- 1 ,要
使1m3该溶液中的NO2- 完全转化为NH4NO3,至少需向装置Ⅳ
中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)


【知识点】化学反应与能量 电化学 F1 F2 F3
【答案解析】
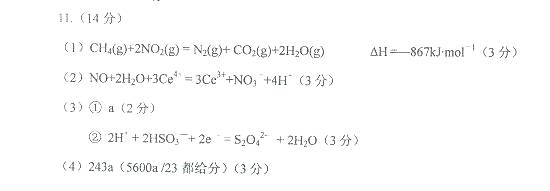
解析:(1)△H=(△H1+△H2)/2,消去NO
(2)NO被氧化为硝酸根,Ce4+被还原为Ce3+,酸性环境,缺氧补水,缺氢补氢离子
(3)生成Ce4+为氧化反应,发生在阳极上,连接电源正极,因此从a口流出
(4)反应物是HSO3-被还原成S2O42-,得到电子
(5)NO2-的浓度为a g•L-1,要使1m3该溶液中的NO2-完全转化为NH4NO3,则失去电子数目是:1000×(5−3)a/46,设消耗标况下氧气的体积是V,则失电子数目是:V÷22.4×2×(2−0),根据电子守恒:
1000a×(5−3)÷46=V÷22.4×2×(2−0),解得V=243a,故答案为:243a.
【思路点拨】本题综合考查学生含氮元素、含硫元素物质的性质知识,注意知识的梳理和归纳是关键,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.32 g O2占有的体积约为22.4 L
B.22.4 L N2含有阿伏加德罗常数个氮气分子
C.在标准状况下,22.4 L水的质量约为18 g
D.22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
某合成气的主要成分是一氧化碳和氢气,可用于合成甲醚等清洁燃料。由天然气获得该合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g)2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g)CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

图1
反应进行的前5 min内,v(H2)=________;10 min时,改变的外界条件可能是______________________________________________________________。
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图像。

(3)反应③中ΔH3=________。800 ℃时,反应③的平衡常数K=1,测得该温度下密闭容器中某时刻各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5 mol | 8.5 mol | 2.0 mol | 2.0 mol |
此时反应③中正、逆反应速率的关系式是________(填代号)。
a.v正>v逆 B.v正<v逆
c.v正=v逆 D.无法判断
(4)用该合成气制取甲醚的化学方程式为______________________________。
该反应的原子利用率为________(设反应完全进行,用质量百分比表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于pH变化的判断正确的是( )
A.温度升,Na2CO3溶液pH减小
B.温度升高,纯水pH增大
C.新制氯水经光照一段时间后,溶液pH减小
D.氢氧化钠溶液久置于空气中,溶液pH变大
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液在25℃时由水电离出的氢离子的浓度为1×10-12 mol·L-1,下列说法正确的是( )
A.HCO 、HS-、HPO
、HS-、HPO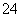 等离子在该溶液中能大量共存
等离子在该溶液中能大量共存
B.该溶液的pH可能为2
C.向该溶液中加入铝片后,一定能生成氢气
D.若该溶液中的溶质只有一种,它一定是酸或者是碱
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)2.00g C2H2完全燃烧生成液态水和CO2,放出99.6kJ热量,请写出表示C2H2燃烧热的热化学方程式:
(2)C2H2可用于制作燃料电池,请写以KOH溶液为电解质溶液的乙炔燃料电池的负极反应式:
(3)用乙炔燃料电池电解AgNO3溶液,用石墨做电解池两极,请写出与电源负极相连的石墨电极的电极反应式:
(4)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn + 2K2FeO4 + 8H2O  3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH
请写出该电池在充电时阴极的电极反应式:
查看答案和解析>>
科目:高中化学 来源: 题型:
英国天文学家在人马座附近发现了一片酒精云,这片酒精云的质量达100万亿亿吨。现有如图转化关系,下列说故不正确的是
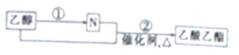
A. N为乙酸
B. 过程①中可加入LiAlH4等还原剂将乙醇转化为N
C. 过程②如果加热一段时间后发现忘记加瓷片,应停止反应,待冷却后补加
D. 可用饱和碳酸钠溶液除去乙酸乙酯中混有的N
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为
(2)钛能与B、C、 N、 O等非金属元素形成稳定的化合物。电负性:C (填“>”或“<”下同)B;第一电离能: N O。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3) 。 FeTiO3与80%的硫酸反应可 生成TiOSO4。SO42-的空间构型为 形,其中硫原子采用 杂化.
(4)磷酸钛〔Ti3 (PO4 )4]锂离子电池能量密度大、安全性高。Ti3 (PO4 )4可由TiOSO4与
 H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
则三分子H3PO4脱去两分子H2O生成三磷酸,其结构式为 ,四分子H3PO4 脱去四分子H2O生成的四偏磷酸属于 元酸。
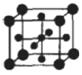
(5)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图所示(Ti4+位于立方体的顶点)。该晶体中,Ti4+和周围 个O2-相紧邻.
(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCI型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1)中,若测得某FexO晶体密度为5.71 g·cm-3,晶胞边长为4.28X10-10 m,则FexO中x=_。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是某药物中间体的结构示意图
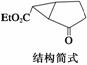
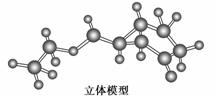
试回答下列问题:
(1)观察上面的结构简式与立体模型,通过对比指出结构简式中的“Et”表示________(填名称);该药物中间体分子的化学式为______________。
(2)请你根据结构示意图,推测该化合物所能发生的反应及所需反应条件__________(写两种)。
(3)解决有机分子结构问题的最强有力手段是核磁共振氢谱(PMR)。有机化合物分子中有几种化学环境不同的氢原子,在PMR中就有几个不同的吸收峰,吸收峰的面积与H原子数目成正比。
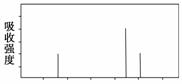
现有一种芳香化合物与该药物中间体互为同分异构体,其模拟的核磁共振氢谱图如上图所示,试写出该化合物的结构简式:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com