
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)  CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c) v(b)>v(d)
C.平衡常数:K(a)>K(c) K(b)=K(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
下列关于四种粒子的结构示意图的说法中正确的是( )
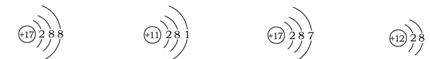
① ② ③ ④
A.①③属于不同种元素 B.④属于离子,离子符号为Mg+2
C.②③的化学性质相似 D.②表示的元素在化合物中通常显+1价
查看答案和解析>>
科目:高中化学 来源: 题型:
A~X七种有机物间转化关系如图所示。其中气体A在标准状况下密度为1.25 g/L,且碳元素的质量分数为85.7%;E普遍存在于许多食物中(如花生、菠菜等);F分子中含有一个六元环,晶体X中仅含C、H、O三种元素,且原子个数比为1:3:3。试回答下列问题:
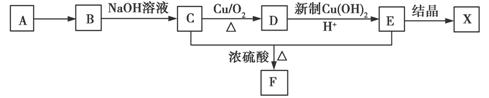
(1)C的结构简式为______________;晶体X的化学式为________________________。
(2)下列转化过程涉及的有机化学反应中,属于取代反应的是________(填序号)。
①A→B ②B→C ③C→D ④D→E ⑤C、E→F
(3)写出D与新制Cu(OH)2悬浊液反应的方程式:_____________________________;
写出C与E生成高分子化合物的化学方程式:____________________________。
(4)简述确定有机物B中官能团的实验方法:________________________________________
_____________________________________________________________________________。
(5)有机物W是F的同系物,具有和F相似的结构,分子组成比F多四个碳原子,也含有六元环,其1H-NMR谱图上只有一个峰,写出一种符合上述条件的W的结构简式:______________________。
(6)有机物Y是一种重要有机化工原料,可制备调香剂、皮肤创伤的愈合剂和某些药品(如头孢)等,Y的分子组成比E少一个氧原子,Y有两种不同的含氧官能团。通过电解方法可由E制取Y,电解槽中阳极通常用石墨,阴极用复合膜电极,采用阳离子交换膜,电解质溶液为饱和E与H2SO4的混合溶液。写出电解槽中阴极的电极反应式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实,找出不能用勒沙特列原理解释的是
A.在溴水中存在如下平衡: ,当加入NaOH溶液后颜色变浅
,当加入NaOH溶液后颜色变浅
B.对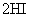

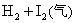 平衡体系增加压强使颜色变深
平衡体系增加压强使颜色变深
C.反应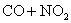

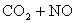 升高温度使平衡向逆方向移动
升高温度使平衡向逆方向移动
D.合成氨反应: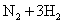

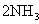 ,为使氨的产率提高,理论上应采取低温高压的措施
,为使氨的产率提高,理论上应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,分别对反应C(s)+CO2(g) 2CO(g)(正向吸热)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是 ( )
2CO(g)(正向吸热)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是 ( )
A.①②③④ B.①③④ C.①② D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.00 mol二氧化硫和1.00 mol氧气通入1.00 L的密闭容器中,分别在500 K,600 K,700 K三个不同的温度下进行2SO2+O2 2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
表一:500 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.10 | 0.15 | 0.20 | 0.25 | 0.30 |
| 时间 | 30 | 35 | 40 | 45 | 50 | 55 |
| SO3浓度(mol·L-1) | 0.35 | 0.40 | 0.50 | 0.55 | 0.60 | 0.60 |
表二:600 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.20 | 0.30 | 0.40 | 0.50 | 0.50 |
表三:700 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.25 | 0.35 | 0.35 | 0.35 | 0.35 |
(1)从上面三个表的数据可以判断该反应是__________反应(填“吸热”或“放热”),利用表一计算0~40 min内用SO2表示该反应的化学反应速率v(SO2)=__________mol·L-1·min-1。
(2)对该反应,下面的说法正确的是__________。
A.当容器中的压强不再变化时,该反应就达到平衡
B.达到平衡时v正(SO2)=v逆(SO3)
C.平衡时c(SO2)=c(SO3)
D.当由500 K平衡状态时升高温度至600 K时,重新达到平衡状态时,容器的压强减小
(3)从上面三个表的数据,温度对该反应的反应速率和平衡移动的影响是_____________________________________________________________________。
(4)计算在600 K时的平衡常数(写出计算过程,最后结果取两位有效数字)。
(5)下图曲线(Ⅰ)是在500 K时SO3浓度的变化曲线,请你在图中画出在550 K进行上述反应的曲线,并标明曲线(Ⅱ)。
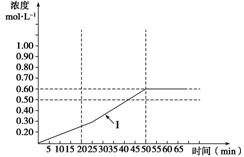
查看答案和解析>>
科目:高中化学 来源: 题型:
有关化学用语正确的是 ( )
A.乙烯的结构简式CH2CH2 B.乙醇的结构简式C2H6O
C.四氯化碳的结构式CCl4 D.乙酸的分子式C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述正确的是 ( )
A.植物油不能发生水解反应 B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应 D.蛋白质水解的产物为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
现有常温时pH=1的某强酸溶液10 mL,下列操作能使溶液pH变成2的是
A.加水稀释成100 mL B.加入10 mL水进行稀释
C.加入10 mL 0.01 mol·L-1的NaOH溶液 D.加入10 mL 0.01 mol·L-1的HCI溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com