
| A. | 含1molFeCl3溶液水解生成1molFe(OH)3胶体后生成NA个胶体粒子 | |
| B. | 分子数为NA的N2,CO混合气体体积为22.4L,质量为28g | |
| C. | 0.5molFeBr2与足量氯气反应转移的电子数为NA | |
| D. | 足量Zn与一定量的浓硫酸反应,产生22.4L标准状况气体时,转移的电子数为2NA |
分析 A.氢氧化铁胶体为多个离子的集合体;
B.气体状况未知;
C.氯气足量二价铁离子、溴离子都被氧化;
D.标准状况下22.4L气体的物质的量为1mol,足量锌与浓硫酸反应生成的气体组成为二氧化硫和氢气,无论生成氢气还是二氧化硫,生成1mol气体都得到2mol电子.
解答 解:A.氢氧化铁胶体为多个离子的集合体,所以含1molFeCl3溶液水解生成1molFe(OH)3胶体后生成小于NA个胶体粒子,故A错误;
B.气体状况未知,Vm不确定,无法计算混合气体的物质的量和质量,故B错误;
C.0.5molFeBr2与足量氯气反应,生成0.5mol三价铁离子,失去0.5mol电子,生成1mol溴单质,失去1mol电子,所以共失去1.5mol电子,转移电子数为:1.5NA,故C错误;
D.足量Zn与一定量的浓硫酸反应,产生的气体为氢气和二氧化硫的混合气体,标准状况下22.4L气体的物质的量为1mol,生成1mol二氧化硫和氢气的混合气体,转移了2mol电子,转移的电子数为2NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的判断及计算,注意明确标况下气体摩尔体积的使用条件,掌握阿伏伽德罗常数与物质的量、摩尔质量等物理量之间的转化关系,题目难度中等.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:多选题
| A. | 150 mL 1 mol•L-1的NaCl | B. | 75 mL 1.5mol•L-1的CaCl2 | ||
| C. | 150 mL 3 mol•L-1的KCl | D. | 75 mL 2 mol•L-1的NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应的能量变化只表现为反应放热或吸热两种形式 | |
| B. | 一个反应的反应物总能量大于生成物总能量,则该反应的焓变一定小于零 | |
| C. | 燃烧热的大小与热化学方程式中可燃物计量系数成正比 | |
| D. | 含1mol硫酸的稀溶液与足量NaOH稀溶液反应生成水所放出的热量为中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的摩尔质量为36.5g | |
| B. | 1mol H2SO4 的质量为98 g.mol-1 | |
| C. | 任何物质的摩尔质量都等于他的相对分子质量或相对原子质量 | |
| D. | CO2 的摩尔质量是H2 的摩尔质量的22倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热为-110.5 kJ•mol-1 | |
| B. | 在101kPa下氢气的燃烧热△H=-285.8 kJ•mol-1,则水分解的热化学方程式:2 H2O (l)=2H2 (g)+O2 (g)△H=+285.8 kJ•mol-1 | |
| C. | Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l)△H=-2akJ•mol-1,则任何强酸和强碱发生中和反应生成1molH2O(l)的反应热均为-akJ•mol-1 | |
| D. | 1g甲烷完全燃烧生成液态水的过程中放出55.6kJ热量,则CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-889.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原混合气体的体积为1.1VL | |
| B. | 原混合气体的体积为1.2VL | |
| C. | 反应达到限度时,气体A消耗掉0.05 VL | |
| D. | 反应达到限度时,气体B消耗掉0.05 VL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
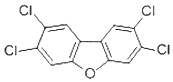 香港食环署食物安全中心日前宣布,两个大闸蟹养殖场样本,被验出二噁英样多氯联苯含量超标.2,4,7,8-四氯二苯并呋喃是其中的一种,结构简式如图,下列有关该物质的说法正确的是( )
香港食环署食物安全中心日前宣布,两个大闸蟹养殖场样本,被验出二噁英样多氯联苯含量超标.2,4,7,8-四氯二苯并呋喃是其中的一种,结构简式如图,下列有关该物质的说法正确的是( )| A. | 能发生氧化反应 | B. | 一溴取代物只有一种 | ||
| C. | 属于氯代芳香烃 | D. | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子从K2FeO4电极沿导线移向Zn电极 | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com