
【题目】工业上冶炼锡的第一步反应原理为2SnO2+3C===2Sn+aM↑+CO2↑,则下列说法中错误的是( )
A. 反应中SnO2被还原
B. a的值为3
C. 反应后元素化合价升高生成的物质有两种
D. 每生成1 mol CO2转移电子8 mol
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】亚氯酸钠是重要漂白剂,大庆市某高中化学实验探究小组设计如下实验制备亚氯酸钠(NaClO2)晶体。
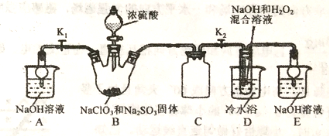
【查阅资料】
I.NaClO2饱和溶液在低于38℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成 NaClO3和NaCl。
II.B中发生的主要反应:2NaClO3+Na2SO3+H2SO4(浓)=2ClO2↑+2Na2SO4+H2O。
【进行实验】
(1)盛装NaClO3和Na2SO3固体的仪器名称是_____。
(2)装置C的作用是____________。
(3)ClO2气体与装置D中混合溶液反应生成NaClO2,生成NaClO2的反应方程式为______。
(4)反应后,经以下步骤可从装置D的溶液获得NaClO2晶体。请补充完整操作。
①55℃蒸发结晶;②趁热过滤;③38-60℃热水洗涤;④低于____干燥,得到成品。
右图是某同学的过滤操作示意图,其操作不规范的是________(填标号)。
a.将滤纸湿润,使其紧贴漏斗壁
b.滤纸边缘高出漏斗边缘
c.用玻璃棒引流
d.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
【实验反思】
(1)如果撤去D中的冷水浴,可能导致产品中混有的杂质是_______。
(2)实验须使B中NaClO3稍微过量,原因是__________,如NaClO3不足,则装置D中可能产生SO42-,检验装置D中是否含有SO42-的方法是:取少量D中反应后的溶液于试管中,__________,证明溶液中存在SO42-。
(3)测定产品中NaClO2的纯度。测定时进行如下实验:
准确称mg样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液。取25.00mL待测溶液,加入淀粉溶液做指示剂,用cmol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。所称取的样品中NaClO2<span lang="EN-US" style="font-size:10.5pt;mso-bidi-font-size:12.0pt;font-family:"Times New Roman","serif";mso-fareast-font-family:"Times New Roman";mso-ansi-language:EN-US;mso-fareast-language:ZH-CN;mso-bidi-language:AR-SA">质量百分含量</span>为_________(用含m、c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各变化中属于原电池反应的( )
A. 在空气中金属铝表面迅速氧化形成保护层
B. 锌与稀硫酸反应时,用锌粉代替锌块可使反应加快
C. 红热的铁丝与冷水接触,表面形成蓝黑色保护层
D. 镀锌铁表面有划损时,仍然能阻止铁被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是六种核电荷数依次增加的短周期元素,它们位于三个不同的周期,B原子的电子数是最内层电子数的三倍,C和E位于同一主族且它们可形成EC2、EC3两种常见化合物,D的最髙价氧化物对应的水化物是强碱,E和F相邻。回答下列问题:
(1)写出B在元素周期表中的位置___________;
(2)写出A、C、F三种元素组成的一种弱电解质的结构式___________;
(3)能说明非金属性F比E强的两个实例_______、___________;
(4)化合物DA遇水会发生剧烈的化学变化,请写出该反应的化学方程式_____________;
(5)金属镁在BC2中燃烧的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯和其他无机原料合成环状酯E和高分子化合物H的示意图如下所示:
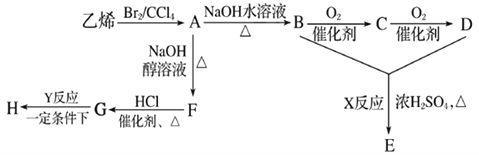
请回答下列问题:
(1)写出以下物质的结构简式:A___________,F___________,C___________。
(2)写出以下反应的反应类型:X_________________,Y__________________。
(3)写出以下反应的化学方程式:A→B:_______________;G→H:___________。
(4)若环状酯E与NaOH水溶液共热,则发生反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物命名及其一氯代物的同分异构体数目均正确的是
命名 | 一氯代物 | |
A | 3—丁炔 | 3 |
B | 1,3-二甲基苯 | 3 |
C | 2-甲基-2-乙基丙烷 | 4 |
D | 2,3-二甲基-4-乙基己烷 | 7 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,对反应CO2(g)+H2(g)![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入体积不变的容器内各组分的物质的量见下表:
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入体积不变的容器内各组分的物质的量见下表:
CO2 | H2 | CO | H2O | |
甲 | 2a mol | 2a mol | 0 | 0 |
乙 | 2a mol | a mol | 0 | 0 |
丙 | 0 | 0 | 2a mol | 2a mol |
丁 | amol | 0 | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A. 乙>丁>甲>丙 B. 乙=丁<丙=甲
C. 丁>乙>丙=甲 D. 丁>丙>乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向FeI2,FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知:2Fe2++Br2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是( )。

A. 线段BD表示Fe3+物质的量的变化
B. 原混合溶液中FeI2的物质的量为1mol
C. 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D. 原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A. 用KIO3氧化酸性溶液中的KI: 5I-+IO3-+3H2O=3I2+6OH-
B. 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
C. 将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+
D. 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com