
����ѧѡ��3�����ʽṹ�����ʡ���80%���ҵķǽ���Ԫ�����ִ�����������Դ�����ܲ��ϵ�����ռ�м�Ϊ��Ҫ�ĵ�λ��
��1�������仯��������������������ϢϢ��أ���̬Nԭ���е�����2p����ϵ��Ų���ѭ��ԭ����__________��N2F2������Nԭ�ӵ��ӻ���ʽ��_____________��1mol N2F2����___________���Ҽ���
��2�������մɲ���Si3N4�����м���N-Si-N___Si-N-Si(�������������=��)��ԭ����__________��
II������Ԫ�����ִ���ҵ��Ҳռ�ݼ�����Ҫ�ĵ�λ����Ҳ����Ϊ��δ���ĸ��������������ᣬ����ʴ��Ӳ�ȴ�����������������豸�ȵ�������ϡ�
��4����̬��ԭ�Ӻ����________���˶�״̬����ͬ�ĵ��ӣ������Ѿ�������ͼ1��ʾ��Ϊ_______�ѻ�(��ѻ���ʽ)��

��5������TiO2��һ��Ӧ�ù㷺�Ĵ����������һ��ʵ������ͼ2���������ҵķе����Ը��ڻ�����ף���Ҫԭ����_____________�����������в�ȡsp3�ӻ���ԭ�ӵĵ縺���ɴ�С��˳��Ϊ_____________��
��6�����ѿ���Ľṹ��ͼ3��ʾ������������ӿ���Ӳ��Ӵ�ģ�ͣ������Ӻ���������������ӵĿ�϶���������γ��������壬������λ�������������ģ���һ�������ӱ�________�������Ӱ�Χ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ����У�������Ĵ�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ʵ����
ʵ��������ͼ��ʾװ���Ʊ�AlC13��Һ������AlC13��Һ�ܽ�һ������CaCO3�γ���Һ�����ð�ˮ������Ȼ����ճ����Ʊ����͵ij������Ϻͷ����������ʮ���� ��12CaO��7Al2O3������֪A1C13��ˮ�⣬��������
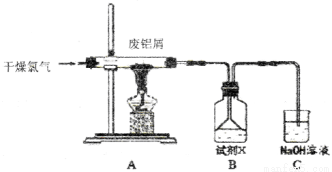
��1����ʵ����������غ�Ũ�����Ʊ������������ӷ���ʽΪ____________��
��Cװ�õ�����____________��
��2�����������м��Ӧ���ɵ�AlC13�����ܽ���B�У�B��ʢ�ŵ��Լ�X��____________��Ϊ�˷�ֹAlC13���������������ܣ�ʵ���пɲ�ȡ�Ĵ�ʩ��____________��д��һ�㣩��
��3��Bװ���е�AlC13��Һ�ܽ�CaCO3ʱ��AlC13��Һ��̼��Ʒ�ĩ�Ļ�Ϸ�ʽΪ____________��
��4��ʵ��Ҫ����̼��ƺ�AlC13������Ҫ��n��CaCO3��: n��A1C13���� 12:14����ԭ����____________��
��5���Թ�ҵ̼��ƣ���������A12O3��Fe2O3���ʣ�������ˮ���Ȼ��ƣ�CaC12��2H2O���ķ���Ϊ������ҵ̼����������ᣬ____________��
��֪�������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol/L���㣩

��ʵ�������õ����Լ��������У����ᣬ�������ƣ���ˮ��pH�ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����5��ģ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�������ֵ�������й�˵����ȷ����
A��1L1mol/L�ļ״�ˮ��Һ�к�����ԭ������Ϊ4NA
B��50mL18.4mol/LŨ����������ͭ�ȷ�Ӧ������SO2���ӵ���ĿΪ0.46NA
C����ӦKIO3+6HI��KI+3H2O+3I2�У�����3molI2ת�Ƶ��ӵ�����Ϊ5NA
D��12gʯī��C60�Ļ��������������Ϊ12NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�����߿���в������ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧѡ��2����ѧ�뼼������̬��ҵ���Ľ��裬�����������ֻ��������Ҫ����ѭ���������ۺͳ�ֿ��Ǿ��õĿɳ�����չ����ͼ��ij��ҵ��Ƶ�����-���-ˮ����������ˮ-��ˮ���á���-��-������������̬��ҵ������ͼ���ش��������⣺
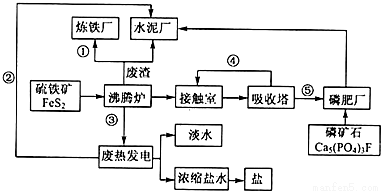
��1����ԭ�ϡ���Դ����ͨ�Ƕȿ��Ǹ���ҵӦ����
A����ɽ�� B�غ����� C������� D������½
��2�������̢١��ڡ��ۡ��ܡ���Ϊ���������ʵ����ͣ���ֱ�д�����͵���Ҫ���ʵĻ�ѧʽ��������ʽ����________����________����________����________����________��
��3������¯������Ӧ�Ļ�ѧ����ʽ__________���ʳ�����Ҫ��Ʒ���ոƣ�����Ҫ�ɷ���___________(�ѧʽ)��
��4���ȵ糧����ȴˮ��________����������Ũ����ˮ����ȡ���������ȡ��������_________��(д��һ�ּ���)
��5�������ִ�������û�������������¯�������������������������ܵ���������______________��(д�����㼴��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�����߿���в������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ܻ���(DCHP)���������ϼӹ�������һ���Ʊ��������£�
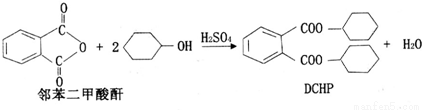
����˵����ȷ����( )
A��DCHP�ķ���ʽΪC20H28O4
B�������Ʊ�DCHP�ķ�Ӧ����ȡ����Ӧ
C��DCHP�����ϵ�һ�ȴ�����4��
D��1molDCHP�����뺬4molNaOH����Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ����ȫ��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ���¶��£�ˮ��Һ��H+��OH-��Ũ�ȱ仯��ͼ��ʾ������˵������ȷ����( )

A�����¶��£�����NaHSO4����������b��a�ı仯
B�����¶��£�pH=2��������pH=12������������Һ�������ϣ�������Һ������
C�����¶��£�����Na2CO3��Һ������b��c�ı仯
D�������¶ȿ�������b��d�ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ǰ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
����ѧ����ѡ��5:�л���ѧ�������й���ѧ���������������ص��о��ٻ���2015��ŵ������ѧ�����������Ǽ��Ұ���ड���ୡ����֮������Ч�Ŀ�ű��Чҩ��������Ч�͵Ͷ����ص㣬��������������֯�����ǡ�������Ψһ��Ч��ű������ҩ����������غϳ�ϵ��������(���ǵ����ƺʹ�����ͼ��ʾ)��·����ͼ��
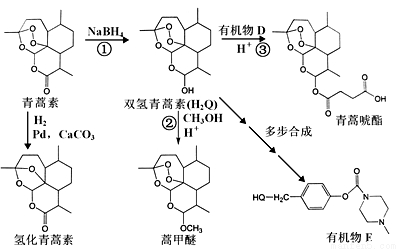
��֪��
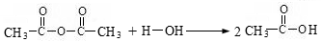
�ش��������⣺
��1�������صķ���ʽΪ_____________________��
��2����Ӧ���У��л���Ӧ����Ϊ___________��NaBH4��������________��(A�������� B����ԭ�� C������ D���ܼ�)
��3���л���D�Ƿ���ʽΪC4H4O3����Ԫ��״�������д��D�Ľṹ��ʽ ��
��4�����ﻣ���ܹ������ķ�Ӧ������ ��
A��������Ӧ B��ˮ�ⷴӦ C����ԭ��Ӧ D���Ӿ۷�Ӧ
��5����H2Q��ʾ˫�������أ�д����Ӧ��(˫�������غͼ״���Ӧ)�Ļ�ѧ����ʽ_________��
��6����˫��������(H2Q)��������ͨ���ಽ��Ӧ�ϳɳ��л���E���ϳɹ����У��л�ԭ�ϳ�H2Q��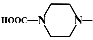 �⣬���躬�����Ķ��ǻ�������F��д���л���F��NaOH��Һ��Ӧ�����ӷ�Ӧ����ʽ___________________________���л���G��F��ͬ���칹�壬�л���G��FeCl3��Һ����ɫ������4�ֲ�ͬ���͵��⣬�������Ϊ3:2:2:1��������������л���G��ͬ���칹����_____�֡�д������һ�ֵĽṹ��ʽ ��
�⣬���躬�����Ķ��ǻ�������F��д���л���F��NaOH��Һ��Ӧ�����ӷ�Ӧ����ʽ___________________________���л���G��F��ͬ���칹�壬�л���G��FeCl3��Һ����ɫ������4�ֲ�ͬ���͵��⣬�������Ϊ3:2:2:1��������������л���G��ͬ���칹����_____�֡�д������һ�ֵĽṹ��ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�캣��ʡ������ǰģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�������ȼ��仯��������ѧ��ѧ��Ҫ����ɲ��֣�
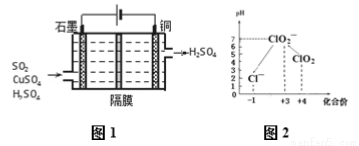
��1������ȼ�ϵ��ʹ�õĵ������Һ�� KOH ��Һ����ط�ӦΪ��4NH3 +3O2 =2N2 +6H2O���õ�ظ����ĵ缫��ӦʽΪ___________���øõ�ؽ��д�ͭ���� Al��Zn��Ag��Pt��Au �����ʣ��ĵ�⾫������CuSO4��ҺΪ�������Һ������˵����ȷ����__________��
a������ȫ��ת��Ϊ��ѧ��
b��SO42�������ʵ���Ũ�Ȳ��䣨��������Һ����仯��
c����Һ��Cu2+�������ƶ�
d������������ɻ���Ag��Pt��Au�Ƚ���
e����������������64g����ת�Ƶ�����Ϊ2NA��
��2����֪KSP��BaSO 4��=1.0��10��10 ��KSP��BaCO3��=2.5��10��9 ��
ijͬѧ�������������̣�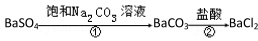 ���õ� BaCl2����ٵ����ӷ���ʽΪ__________________���÷�Ӧ��ƽ�ⳣ��K=__________��
���õ� BaCl2����ٵ����ӷ���ʽΪ__________________���÷�Ӧ��ƽ�ⳣ��K=__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶�6���¿���ѧ�Ծ��������棩 ���ͣ������
��KMnO4����������������Ϊ36.5%�����ᡣ��Ӧ����ʽ���£�
2KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O
��1������������ܶ�Ϊ1.2g/cm3�������ʵ���Ũ��Ϊ_________________________��
��2����˫���ű�ʾ���ӵĵ�ʧ_________________________��
��3���˷�Ӧ����������_________����������____________��
��4������xmolKMnO4�μӷ�Ӧ����ת�Ƶ��ӵ����ʵ���Ϊ____________��
��5��15.8gKMnO4��ȫ��Ӧ��������״����Cl2�����Ϊ_________��ͬʱ��________molHCl��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com