
在恒温、恒容的密闭容器中进行反应A(g)B(g)+C(g),若反应物的浓度由2 mol·L-1降到0.8 mol·L-1需要20 s,那么反应物浓度再由0.8 mol·L-1降到0.2 mol·L-1所需要的时间为( )
A. 10 s B.大于10 s
C.小于10 s D.无法判断
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列关于0.2 mol·L-1K2SO4溶液的正确说法是
( )
A.1 L溶液中K+浓度是0.4 mol·L-1
B.溶液中含有0.4NA个K+
C.1 L溶液中所含K+、S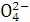 总数为0.3NA
总数为0.3NA
D.2 L溶液中S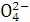 浓度是0.4 mol·L-1
浓度是0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
未来新能源的特点是来源丰富,在使用时对环境无污染或污染很小,且可以再生。下列满足未来新能源标准的是( )
①天然气 ②煤 ③石油 ④太阳能 ⑤生物质能
⑥风能 ⑦氢
A.①②③④ B.④⑤⑥⑦
C.③⑤⑥⑦ D.③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
士兵在野外加热食物时通常采用“无焰食物加热器”,其主要化学成分为镁粉、铁粉、氯化钠粉末。使用时加入水与其中的镁反应放出热量。下面是在室温下对本产品的两个探究实验。
实验1:向加有等量水的三个相同隔热容器中分别加入下列各组物质,结果见下图。
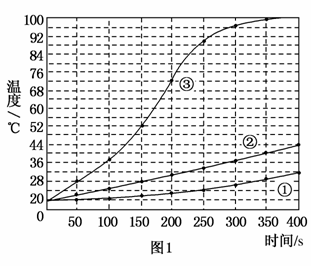
①1.0 mol镁条、0.10 mol铁粉、0.10 mol氯化钠粉末;
②将1.0 mol镁条剪成100份、0.10 mol铁粉、0.10 mol 氯化钠粉末;
③1.0 mol镁粉、0.10 mol 铁粉、0.10 mol氯化钠粉末;
实验2:向加有100 mL水的多个相同的隔热容器中分别加入由0.10 mol镁粉、0.50 mol铁粉及不同量的氯化钠粉末组成的混合物,不断搅拌,第15 min时记录温度升高的幅度,结果见图2。
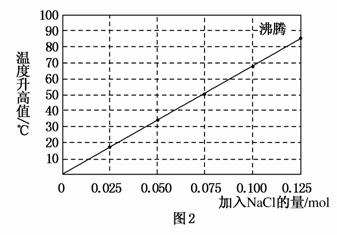
请回答下列问题:
(1)实验1证实了该反应的反应速率与________有关。
(2)实验2中当NaCl的用量大于0.125 mol时,实验就无须再做的原因是________(填选项字母)。
A.加入更多的NaCl不再增加反应速率
B.加入NaCl反而会降低反应速率
C.已达到沸点不再有温度变化
D.需要加入更多的铁粉来提高温度
(3)如果在实验2中加入0.060 mol的NaCl,则第15 min时混合物的温度最接近于________(填字母)。
A.34 ℃ B.42 ℃
C.50 ℃ D.62 ℃
(4)加入铁粉和NaCl能使反应速率加快的原因是_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.一定条件下可以用H2除去乙烷中混有的乙烯
B.苯和四氯化碳都能萃取溴水中的溴
C.乙醇、乙酸和乙酸乙酯三者的混合液可用分液的方法分离
D.甲烷、乙烯和苯在工业上都可通过石油分馏得到
查看答案和解析>>
科目:高中化学 来源: 题型:
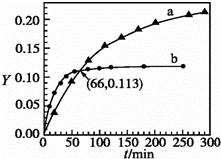
已知反应:2CH3COCH3(l)⇌CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y﹣t)如图所示.下列说法正确的是( )
|
| A. | b代表0℃下CH3COCH3的Y﹣t曲线 |
|
| B. | 反应进行到20min末,CH3COCH3的 |
|
| C. | 升高温度可缩短反应达平衡的时间并能提高平衡转化率 |
|
| D. | 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
两个化学兴趣小组进行了以下探究活动:
第一组:为研究铁质材料与热浓硫酸的反应,
(1)称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为 (选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为 。
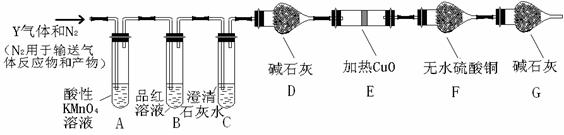 分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(2)写出产生CO2的化学方程式 。
(3)装置A中试剂的作用是 ,反应的离子方程式 。
(4)简述确认气体Y中含有CO2的实验现象 。
(5)如果气体Y中含有H2,预计实验现象应是 。
第二组:拟用下列装置定量分析空气中SO2的含量:
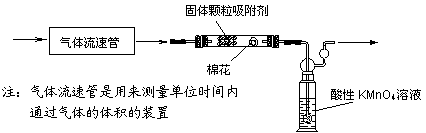
(6)KMnO4溶液中导管末端做成球状多孔结构的作用是
(7)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为 g/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com