
【题目】实验室用氢氧化钠溶液、铁屑、稀硫酸等试剂制备氢氧化亚铁沉淀,其装置如图所示。
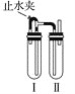
(1)在试管Ⅰ里加入的试剂是____________________。
(2)在试管Ⅱ里加入的试剂是____________________。
(3)为了制得白色氢氧化亚铁沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是______________________________________。
(4)这样生成的氢氧化亚铁沉淀能较长时间保持白色,其理由是_________________________。
【答案】稀硫酸、铁屑 氢氧化钠溶液 如果Ⅱ中试管有连续均匀气泡产生,可确定已排净空气,再夹紧止水夹 试管Ⅰ中反应生成的氢气充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入
【解析】
(1)试管I内铁与硫酸反应生成硫酸亚铁和氢气;
(2)根据试管Ⅱ中产生氢氧化亚铁分析;
(3)根据需要将生成的硫酸亚铁压入试管Ⅱ内与氢氧化钠反应生成白色的氢氧化亚铁沉淀分析;
(4)铁与硫酸反应生成硫酸亚铁和氢气,此时打开止水夹,氢气进入试管Ⅱ,排除装置内的空气。
(1)若要在该装置中得到Fe(OH)2白色絮状沉淀,先打开止水夹,试管I内铁与硫酸反应生成硫酸亚铁和氢气,把导管中的空气排入试管Ⅱ中,并且通过出气口排出,使氢氧化亚铁不能与氧气充分接触,从而达到防止被氧化的目的,所以试管A中加入的试剂是稀H2SO4、Fe屑;
(2)试管Ⅱ内产生氢氧化亚铁沉淀,则试管Ⅱ中加入的试剂是NaOH溶液;
(3)由于要排尽装置中的空气,且需要把试管Ⅰ中产生的硫酸亚铁排入试管Ⅱ中,则在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是如果Ⅱ中试管有连续均匀气泡产生,可确定已排净空气,再夹紧止水夹;
(4)铁与硫酸反应生成硫酸亚铁和氢气,此时打开止水夹,氢气进入试管Ⅱ,排除装置内的空气,即由于试管Ⅰ中反应生成的氢气充满了试管Ⅰ和试管Ⅱ,且外界空气不容易进入,所以生成的氢氧化亚铁沉淀能较长时间保持白色。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)![]() MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s)+SO2(g)+ CO2(g) ΔH>0,该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
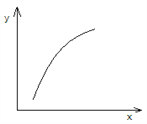
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅蓄电池的工作原理为Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O,现用如图装置进行电解(电解液足量),电解中发现Ag电极有气体产生。请回答下列问题。
2PbSO4+2H2O,现用如图装置进行电解(电解液足量),电解中发现Ag电极有气体产生。请回答下列问题。

甲池 乙池
(1)B是铅蓄电池的________极,放电过程中A电极反应式:_______________________。
(2)电解后甲池中电解液的pH________(填“减小”“增大”或“不变”)。若甲池中产生气体11.2L(标准状况下),此时乙池中理论上Zn电极最多产生固体________ g。
(3)乙池中 C(碳)电极是_________极。C电极的电极反应式是___________________,反应一段时间后,向乙池中加入一定量的___________(填化学式)固体,能使CuSO4溶液恢复到原浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A和E可以合成芳香酯I,合成路线如图所示:
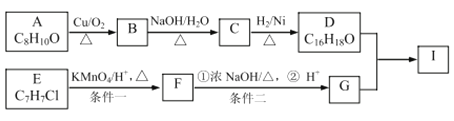
已知:
①![]()
②2RCH2CHO![]()
③B的苯环上只有一个取代基,且能发生银镜反应;
④E的核磁共振氢谱有3组峰
请回答下列问题:
(1)A的结构简式为________,B的化学名称是________ 。
(2)C→D的反应类型为________,F中所含官能团的名称是________ 。
(3)条件一与条件二能否互换____(填“能”或“否”),原因是_________ 。
(4)写出D与G反应的化学方程式_______________ 。
(5)A的同分异构体很多,其中能使FeCl3溶液显紫色有___种,写出其中一种核磁共振氢谱有4组峰的分子的结构简式________ 。
(6)结合题中信息,写出以溴乙烷为原料制备1-丁醇的合成路线图______ (无机试剂任选),合成路线流程图示例如下:![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用蒸馏水稀释1mol/L氨水至0.01mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是
A. c(OH-)/ c(NH3·H2O) B. c(NH![]() )/ c(OH-)
)/ c(OH-)
C. c(NH3·H2O)/ c(NH![]() ) D. c(OH-)
) D. c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置说法正确的是
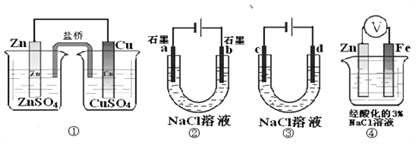
A. 装置①中,盐桥中的Cl-移向CuSO4溶液
B. 装置②工作一段时间后,a极表面生成了较多的O2
C. 用装置③精炼铜时,c极为粗铜
D. 装置④中电子由Zn流向Fe,Zn极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4﹣O2燃料电池具有放电稳定,无污染等优点,如图用甲烷氧气燃料电池电解饱和氯化钠溶液的模型图,其中氯化钠溶液滴有酚酞试液。已知甲烷氧气燃料电池的总反应式为:CH4+2O2+2KOH K2CO3+3H2O请认真读图,回答以下问题:
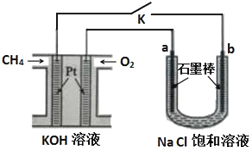
(1)请写出通入甲烷气体的一极所发生的电极反应式:____________________,其附近的pH值________(填“不变”或“变大”或“变小”) 通入O2气体的一极所发生的电极反应式:_______________,其附近的pH值________(填“不变”或“变大”或“变小”)。
(2)a为_______极,电极反应式为______________;b为_______极,电极反应式为_________________,现象是_______________;总方程式为 ____________________________。
(3)如果通入1mol的甲烷完全参与电极反应,则电路中转移___________mol的电子,a电极产生的气体在标准状况下的体积为______________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是()
A. ![]() 、
、 ![]() 是质量数和电子数相等的两种微粒,中子数也相等
是质量数和电子数相等的两种微粒,中子数也相等
B. ![]() 原子的质子数与中子数差50
原子的质子数与中子数差50
C. 35Cl和37Cl两者互为同位素
D. 当氘原子转变为氕原子发生了分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/ L NaOH 溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和20.00 mL 0.1000 mol/LCH3COOH溶液,得到2 条滴定曲线,如下图所示:
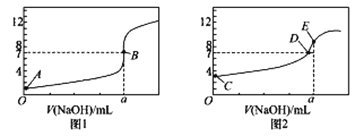
(1)由A、C点判断,滴定HCl溶液的曲线是_____(填“图1”或“图2”);
(2)a=____ mL;
(3)c(Na+ )=c(CH3COO-)的点是_________;
(4)E点对应离子浓度由大到小的顺序为___________________________。
(5)当NaOH 溶液滴定CH3COOH 溶液过程中,NaOH溶液消耗了10.00 mL时,则此时混合液中c(CH3COOH)____c (CH3COO-)(“>”或“<”或“=” )。
(6)在25℃ 时,将c mol/L的醋酸溶液与0.2mol/LNaOH溶液等体积混合后溶液恰好星中性,用含c 的代数式表示CH3COOH 的电离常数Ka=___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com