
(1)�뽫�����������ʣ�KBr��Br2��I2��KI��K2SO4�ֱ��������к����ϣ����һ��δ��ƽ�Ļ�ѧ����ʽ��
KBrO3�� ��H2SO4���� �� �� �� ��H2O��
(2)����û�ѧ����ʽ��I2��KBr�Ļ�ѧ�������ֱ���8��1�����Br2�Ļ�ѧ�������� ��
���뽫��Ӧ��Ļ�ѧʽ����ƽ��Ļ�ѧ����������������Ӧ��λ���У�
KBrO3�� �� H2SO4����������
����ת��10 mol���ӣ���Ӧ������I2�����ʵ���Ϊ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������NO�ķ�Ӧԭ��Ϊ��2CO��2NO=N2��2CO2�йظ÷�Ӧ��˵������ȷ���� ( )
| A����Ӧ��COΪ������ |
| B����Ӧ��NO����ԭ |
| C���ڷ�Ӧ����1 mol N2ʱ��ת�Ƶĵ���Ϊ4 mol |
| D��CO��NO������ɫ�ж����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
þ�Ǻ�ˮ�к����϶�Ľ�����þ��þ�Ͻ���þ�Ļ������ڿ�ѧ�о���ҵ��������;�dz��㷺��
��1��Mg2Ni��һ�ִ���Ͻ���֪��
Mg(s) + H2(g)=MgH2(s) ��H1=��74.5kJ��mol��1
Mg2Ni(s) + 2H2(g)=Mg2NiH4(s) ��H2=��64.4kJ��mol��1
Mg2Ni(s)+2MgH2(s) = 2Mg(s)+Mg2NiH4(s) ��H3
���H3 = kJ��mol��1��
��2����ҵ�Ͽ��õ�����ڵ���ˮ�Ȼ�þ���þ�������Ȼ�þ��ˮ�ǹؼ�����֮һ��һ������������Ȼ�þ������ˮ�ķ����ǣ��Ƚ�MgCl2��6H2Oת��ΪMgCl2��NH4Cl��nNH3���þ���Σ�,Ȼ����700���Ѱ��õ���ˮ�Ȼ�þ���Ѱ���Ӧ�Ļ�ѧ����ʽΪ ����������Ȼ�þ�������ĵ缫��ӦʽΪ ��
��3���������Mg(AlH4)2��110-200��C�ķ�ӦΪ��Mg(AlH4)2=MgH2 +2A1+3H2��ÿ����27gAlת�Ƶ��ӵ����ʵ���Ϊ ��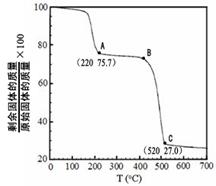
��4����ҵ����MgC2O4��2H2O�ȷֽ��Ƴ�ϸMgO�����ȷֽ�������ͼ��
ͼ�и�������������B��C������Ӧ�Ļ�ѧ����ʽΪ ��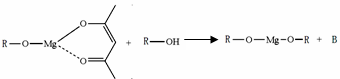
��5��һ���л�þ����������������ѧԪ����Ϳ��Һ����ѧʽ�ɱ�ʾΪ��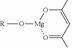 �����ɷ������·�Ӧ��
�����ɷ������·�Ӧ��
ROH��B�ĺ˴Ź�����������ͼ: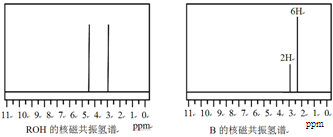
ROH��C��H��O��F����Ԫ����ɵĺ����л��������ֻ��1����ԭ�ӣ����з�ԭ�ӻ�ѧ������ͬ����Է�������Ϊ168����ROH�Ľṹ��ʽΪ �� B�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��50 mL a mol��L��1��������Һ�У�����6��4 g Cu������ȫ���ܽ⣬�һ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100 mL�����c(NO3-)��4 mol��L��1��
��1��ϡ�ͺ����Һ��c(H+)�� mol��L��1
��2����a��10�������ɵ�������NO2�����ʵ���Ϊ________mol
��3����������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2��NO��2NaOH=2NaNO2��H2O 2NO2��2NaOH=NaNO2��NaNO3��H2O
������������屻1 mol��L��1��NaOH��Һǡ�����գ���NaOH��Һ�����Ϊ________mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���û��ϼۺ���������Ʋ����ʵ������ǻ�ѧ�о�����Ҫ�ֶΡ�
��1���ӻ��ϼ۵ĽǶȿ���Ԥ�����ʵ����ʡ�
�ٽ�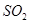 ͨ������
ͨ������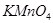 ��Һ�У���Һ����ɫ������ɫ����Ӧ��������Ԫ�ش�����ʽ�������� ��
��Һ�У���Һ����ɫ������ɫ����Ӧ��������Ԫ�ش�����ʽ�������� ��
| A��S2- | B��S | C��SO32- | D��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
L��M��R��P��Q�ֱ�������ֺ���ͬ���ϼ۵ĵ�Ԫ�ص����ʡ�A��B�ֱ�������ֺ���ͬ���ϼ۵���Ԫ�ص�����(ÿ�������е�����Ԫ�صĻ��ϼ�ֻ��һ��)����֪����M�еĵ�Ԫ�ػ��ϼ�Ҫ������Q�е�Ԫ�صĻ��ϼ۵͡���һ�������£����ǻᷢ�����µ�ת��(��ϵʽδ��ƽ)��
��P��A�D��Q��B����L��O2�D��M��H2O����L��M�D��R��H2O����B��H2O�D��A��O2
(1)�����ֺ���Ԫ�ص������У���һ�������ᣬ�������� �������� ��
(2)��Ӧ�ڱ����ڴ���(������������)�����£����ȵ�һ���¶�ʱ���ܷ������˷�Ӧ�ڻ�������������Ҫ��;���ݴ��ƶ���ͬ��ͬѹ�£�������R�ܶȱȿ������ܶ�С����R�Ļ�ѧʽΪ ��
(3)ijͬѧд���������������������ת���Ĺ�ϵʽ��
��.M��P�D��N2O3��H2O
��.N2O4��H2O�D��P��Q
��.M��L�D��Q��H2O
����һ��������ʵ�ֵ��� �������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
A��B��C��D��F�dz����Ļ��������F�ڳ�������һ����ɫҺ�壬DΪǿ�ᣬ�������ͼת����ϵ����Ӧ���������ֲ�������ȥ�����ش��������⣺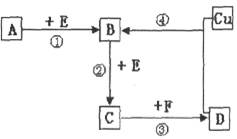
��1����A��B��C��D��Ϊ����Ԫ�صĻ����A��һ�ֳ����Ŀ�ʯ����Ҫ�ɷ֣���A��Ħ������Ϊ120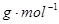 �� ��Ӧ�ٵĻ�ѧ����ʽΪ ��
�� ��Ӧ�ٵĻ�ѧ����ʽΪ ��
��2����A��B��C��D��Ϊ����Ԫ�صĻ������A��һ��������ֻ����10�����ӣ���
��A����ʽΪ__________��
�ڷ�Ӧ�ܵ����ӷ���ʽΪ________________________________________________
��ȡCu��Cu2O�Ļ������Ʒ12��0g�����뵽������D��ϡ��Һ�У�����ˮ���ռ����������壬��״���������Ϊ2��24L������Ʒ��Cu2O������Ϊ__________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
Ϊ֤��Fe3+���н�ǿ�������ԣ���ͬѧ��������ʵ�飺��CuƬ����0.5mol/L Fe(NO3)3��Һ�У��۲쵽CuƬ���ܽ⣬��Һ�ɻ�ɫ��Ϊ����ɫ���ɴ˼�ͬѧ�õ�Fe3+���н�ǿ�����ԵĽ��ۡ�
��ͬѧ����˲�ͬ�Ŀ�������Fe(NO3)3��Һ�������ԣ��ڴ�����������NO3-Ҳ������Cu���������ʵ�����̽������֪��
| ˮ�ⷴӦ | ƽ�ⳣ����K�� |
Fe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ | 7.9 �� 10-4 |
Fe2+ + 2H2O  Fe(OH)2 + 2H+ Fe(OH)2 + 2H+ | 3.2 �� 10-10 |
Cu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+ | 3.2 �� 10-7 |
| ʵ������ | ʵ������ |
| ��ͬѧ��ʵ�鷽�� | ��Һ�������ɫ�� pH�������� |
| ��ͬѧ��ʵ�鷽�� | ����������pHû�����Ա仯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
MnO2��KMnO4������ѧ��ѧ�еij����Լ�����ش��������⣺
��1��MnO2��H2O2�ֽⷴӦ��������������MnO2�����ữ��H2O2��Һ�У�MnO2 �ܽ����Mn2+����Ӧ�����ӷ���ʽ�� ��
��2����MnO2��KMnO4�Ĺ���������ͼ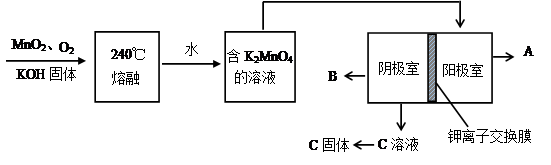
�������������Ͼ�Ϊ̼������ˮ��������Һ��K2MnO4�����绯�����MnO2��KMnO4��
��д��240������ʱ������Ӧ�Ļ�ѧ����ʽ ��Ͷ��ʱ��������n(KOH)��n(MnO2) ��
�������ĵ缫��ӦΪ ��
��B������ ��д��ѧʽ����ͬ��������ѭ��ʹ�õ������� ��
�ܼ����ӽ���Ĥ��һ�ֲ����Ǿ۱�ϩ��أ�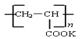 �����۱�ϩ��ص���Ľṹ��ʽΪ ��
�����۱�ϩ��ص���Ľṹ��ʽΪ ��
�������Ƶõ�KMnO4��Ʒ0.165 g��ǡ����0.335 g�������ữ��Na2C2O4��Ӧ��ȫ����KMnO4��
������ ����ȷ��0.1%����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com