
”¾ĢāÄæ”æ³£ĪĀŹ±£¬Ļņ120 mL 0.005 mol”¤L£1 CaCl2ČÜŅŗÖŠÖšµĪ¼ÓČė0.1 mol”¤L£1 Na2CO3ČÜŅŗ£¬»ģŗĻČÜŅŗµÄµēµ¼ĀŹ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£ŅŃÖŖ25”ꏱ£¬Ksp(CaCO3)=3.36”Į10£9£¬ŗöĀŌCO32-Ė®½ā”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
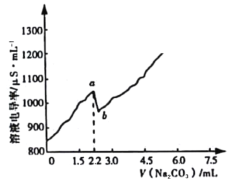
A.aµć¶ŌÓ¦µÄČÜŅŗÖŠCa2+æŖŹ¼ŠĪ³É³Įµķ£¬ČÜŅŗÖŠc(Ca2+)=c(CO32£)
B.bµć¶ŌÓ¦µÄČÜŅŗÖŠCa2+ŅŃĶźČ«³Įµķ£¬ĒŅ“ęŌŚ¹ŲĻµ£ŗc(Na+)+c(H+)=c(Cl£)+c(OH£)
C.ŌŚµĪ¼ÓNa2CO3ČÜŅŗµÄ¹ż³ĢÖŠ£¬»ģŗĻČÜŅŗµÄpHĻČ¼õŠ”ŗóŌö“ó
D.ÓŅĶ¼æÉŅŌĖµĆ÷CaCO3ŌŚČÜŅŗÖŠ“ęŌŚ¹ż±„ŗĶĻÖĻó
”¾“š°ø”æD
”¾½āĪö”æ
A£®ÓÉĶ¼æÉÖŖ£¬aµć¶ŌÓ¦µÄČÜŅŗµ¼µēÄÜĮ¦¼±¾ēĻĀ½µ£¬ĖµĆ÷Ca2£«æŖŹ¼ŠĪ³É³Įµķ£¬¶ųČÜŅŗÖŠµÄøĘĄė×ÓŗĶĢ¼ĖįøłĄė×Ó·Ö±šĄ“Ō“ÓŚCaCl2ČÜŅŗŗĶNa2CO3ČÜŅŗ£¬CaCO3ŠĪ³É³ĮµķŹ±£¬Ca2£«ŗĶCO32£²»Ņ»¶ØĻąµČ£¬¹ŹA“ķĪó£»
B£®ŌČÜŅŗÖŠn£ØCa2£«£©=120mL”Į0.005mol”¤L£1=0.6mmol£¬ŅŖŹ¹øĘĄė×ÓĶźČ«³Įµķ£¬ŠčŅŖĢ¼ĖįÄĘČÜŅŗµÄĢå»żĪŖ![]() =6mL£¬ĻņbµćÖŠ¶ŌÓ¦µÄČÜŅŗÖŠ¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żŠ”ÓŚ6mL£¬²»ÄÜŹ¹øĘĄė×ÓĶźČ«³Įµķ£¬µēŗÉŹŲŗć¹ŲĻµŹ½ĪŖ£ŗ2c£ØCa2£«£©+c£ØNa£«£©+c£ØH£«£©=c£ØCl££©+c£ØOH££©+2c£ØCO32££©£¬¹ŹB“ķĪó£»
=6mL£¬ĻņbµćÖŠ¶ŌÓ¦µÄČÜŅŗÖŠ¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żŠ”ÓŚ6mL£¬²»ÄÜŹ¹øĘĄė×ÓĶźČ«³Įµķ£¬µēŗÉŹŲŗć¹ŲĻµŹ½ĪŖ£ŗ2c£ØCa2£«£©+c£ØNa£«£©+c£ØH£«£©=c£ØCl££©+c£ØOH££©+2c£ØCO32££©£¬¹ŹB“ķĪó£»
C£®²»ŗöĀŌCO32£Ė®½āµÄĒéæöĻĀ£¬ŌŚ¼ÓČėĢ¼ĖįÄĘČÜŅŗŗóƻӊ³ĮµķĪö³ö£¬ČÜŅŗpH±ä“ó£¬Īö³öĢ¼ĖįøĘŹ±£¬ČÜŅŗµÄpHĶ»Č»±äŠ”£¬ŌŚCa2£«ĶźČ«³ĮµķÖ®Ē°£¬»ģŗĻČÜŅŗµÄpHÖµ¼øŗõ²»±ä£¬µ±ĖłÓŠµÄøĘĄė×Ó×Ŗ»ÆĪŖĢ¼ĖįøĘ³Įµķŗ󣬼ĢŠųµĪ¼ÓĢ¼ĖįÄĘČÜŅŗ£¬ČÜŅŗµÄpHÖµ±ä“ó£¬Ö±ÖĮÓėĢ¼ĖįÄĘČÜŅŗµÄpH¼øŗõĻąĶ¬£¬ŗöĀŌCO32£Ė®½āµÄĒéæöĻĀ£¬Ė®ČÜŅŗµÄpH²»·¢Éś±ä»Æ£¬¹ŹC“ķĪó£»
D£®ĄķĀŪÉĻCa2£«æŖŹ¼ŠĪ³É³Įµķ£¬c£ØCO32££©”Ö![]() mol”¤L£1”Ö10-6mol”¤L£1£¬¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żĪŖ
mol”¤L£1”Ö10-6mol”¤L£1£¬¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żĪŖ![]() ”Ö10-2mL£¬¼“1µĪĢ¼ĖįÄĘČÜŅŗ¾ĶÄÜŹ¹ČÜŅŗÖŠµÄĄė×Ó»ż£¾Ksp£ØCaCO3£©£¬¶ųĻņaµć¶ŌÓ¦µÄČÜŅŗ¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żĪŖ2.2ml£¬“ĖŹ±£¬ČÜŅŗ“¦ÓŚ¹ż±„ŗĶČÜŅŗ£¬¹ŹDÕżČ·£»
”Ö10-2mL£¬¼“1µĪĢ¼ĖįÄĘČÜŅŗ¾ĶÄÜŹ¹ČÜŅŗÖŠµÄĄė×Ó»ż£¾Ksp£ØCaCO3£©£¬¶ųĻņaµć¶ŌÓ¦µÄČÜŅŗ¼ÓČėĢ¼ĖįÄĘČÜŅŗµÄĢå»żĪŖ2.2ml£¬“ĖŹ±£¬ČÜŅŗ“¦ÓŚ¹ż±„ŗĶČÜŅŗ£¬¹ŹDÕżČ·£»
¹ŹŃ”D”£


 ÖĒȤŗ®¼Ł×÷ŅµŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
ÖĒȤŗ®¼Ł×÷ŅµŌĘÄĻæĘ¼¼³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²ÉÓƵē»Æѧ·½·ØŅŌSO2ŗĶNa2SO3ĪŖŌĮĻÖĘČ”ĮņĖįµÄ×°ÖĆČēĶ¼ĖłŹ¾(A”¢BĪŖ¶ąæ׏ÆÄ«µē¼«£¬C”¢DĪŖ¶čŠŌµē¼«)”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø £©

A.”°Ä¤2”±ĪŖŃōĄė×Ó½»»»Ä¤
B.µē¼«AµÄµē¼«·“Ó¦ĪŖSO2£2e-+2H2O==SO42-+4H+
C.ÉĻŹö¹ż³ĢÖŠ£¬ŃĒĮņĖįÄĘČÜŅŗæÉŃ»·Ź¹ÓĆ
D.Ź¹ÓĆøĆ×°ÖĆÖĘČ”98gĮņĖįŠčĻūŗÄ11.2L O2(STP)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖX(g)£«3Y (g)![]() 2W(g) £«M (g) ”÷H£½£a kJ”¤mol£1£Øa>0£©”£Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚĢå»żŗć¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1 mol X(g) Óė1mol Y (g)£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
2W(g) £«M (g) ”÷H£½£a kJ”¤mol£1£Øa>0£©”£Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚĢå»żŗć¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬¼ÓČė1 mol X(g) Óė1mol Y (g)£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ³ä·Ö·“Ó¦ŗ󣬷ųöČČĮæĪŖa kJ
B. µ±·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬XÓėWµÄĪļÖŹµÄĮæÅضČÖ®±ČŅ»¶ØĪŖ1£ŗ2
C. µ±XµÄĪļÖŹµÄĮæ·ÖŹż²»ŌŁøı䣬±ķĆ÷øĆ·“Ó¦ŅŃ“ļĘ½ŗā
D. ČōŌö“óYµÄÅØ¶Č£¬Õż·“Ó¦ĖŁĀŹŌö“ó£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪ¬ÉśĖŲCÓÖ³Ęæ¹»µŃŖĖį£¬ÄÜŌöĒæ¶Ō“«Č¾²”µÄµÖæ¹Į¦£¬ÓŠ½ā¶¾×÷ÓĆµČ£¬Ęä½į¹¹Ź½ĪŖ £¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ
£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ
A.Ī¬ÉśĖŲC·Ö×ÓŹ½ĪŖC6H8O6
B.Ī¬ÉśĖŲCµÄĶ¬·ÖŅģ¹¹ĢåÖŠæÉÄÜÓŠ·¼Ļć×å»ÆŗĻĪļ
C.ĻņĪ¬ÉśĖŲCČÜŅŗÖŠµĪ¼Ó×ĻÉ«ŹÆČļŹŌŅŗ£¬ČÜŅŗŃÕÉ«±äŗģ£¬ĖµĆ÷Ī¬ÉśĖŲCČÜŅŗĻŌĖįŠŌ
D.ŌŚŅ»¶ØĢõ¼žĻĀ£¬Ī¬ÉśĖŲCÄÜ·¢ÉśŃõ»Æ·“Ó¦”¢¼Ó³É·“Ó¦”¢Č”“ś·“Ó¦ŗĶĻūČ„·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±½ŅŅĶŖ³£ĪĀĻĀĪŖĪŽÉ«¾§Ģå»ņĒ³»ĘÉ«ÓĶדŅŗĢ壬ŹĒɽ體¢ŗ¬Šß²Ż”¢×Ļ¶”ĻćµČĻć¾«µÄµ÷ŗĻŌĮĻ£¬²¢¹ć·ŗÓĆÓŚŌķÓĆĻć¾«ŗĶŃĢ²ŻĻć¾«ÖŠ£¬æÉÓɱ½¾ĻĀŹö·“Ó¦Öʱø£ŗ
![]() +(CH3CO)2O(ŅŅĖįōū)
+(CH3CO)2O(ŅŅĖįōū) ![]() +CH3COOH£¬ NA“ś±ķ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
+CH3COOH£¬ NA“ś±ķ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A.1 mol±½Ėłŗ¬µÄ»Æѧµ„¼üŹżÄæĪŖ12NA
B.0.1 molŅŅĖįōūÖŠŗ¬ÓŠµÄµē×ÓŹżÄæĪŖ5.4NA
C.ĘųĢ¬±½ŅŅĶŖµÄĆܶȏĒĘųĢ¬ŅŅĖįĆܶȵÄ2±¶
D.1L 2 mol”¤L£1 CH3COOHČÜŅŗÓė×ćĮæÄĘ·“Ӧɜ³ÉµÄĘųĢå·Ö×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄĘ”¢Ģś¼°ĖüĆĒµÄ»ÆŗĻĪļŌŚÉś²ś”¢Éś»īÖŠÓŠ×ÅÖŲŅŖµÄÓĆĶ¾”£
£Ø1£©Ä³Ęū³µ°²Č«ĘųÄŅµÄ²śĘųŅ©¼ĮÖ÷ŅŖŗ¬ÓŠNaN3”¢Fe2O3”¢KClO4”¢NaHCO3µČĪļÖŹ”£µ±Ęū³µ·¢ÉśÅöײŹ±£¬NaN3ŃøĖŁ·Ö½ā²śÉśN2ŗĶNa£¬Ķ¬Ź±·Å³ö“óĮæµÄČČ”£N2Ź¹ĘųÄŅŃøĖŁÅņÕĶ£¬“Ó¶ųĘšµ½±£»¤×÷ÓĆ”£KClO4ÖŠĀČŌŖĖŲµÄ»ÆŗĻ¼ŪŹĒ_________£¬¾ßÓŠ_________£ØĢī”°»¹ŌŠŌ”±»ņ”°Ńõ»ÆŠŌ”±£©£»Fe2O3æÉ“¦Ąķ²śÉśµÄNa£¬·“Ó¦ĪŖ6Na + Fe2O3 =3Na2O + 2Fe£¬·“Ó¦ÖŠNa×ö_________£ØĢī”°»¹Ō¼Į”±»ņ”°Ńõ»Æ¼Į”±£©”£
£Ø2£©¼×”¢ŅŅĮ½Ķ¬Ń§ÓūÖĘČ”“æ¾»µÄFe(OH)2 £¬øł¾ŻČēĶ¼ĖłŹ¾µÄ×°ÖĆ½ųŠŠŹŌŃ锣A¹ÜÖŠŹĒFe·ŪŗĶĻ”H2SO4 £¬ B¹ÜÖŠŹĒNaOHČÜŅŗ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
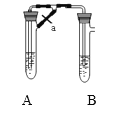
¢ŁĶ¬Ń§¼×£ŗĻČ¼Š½ōÖ¹Ė®¼Ša£¬Ź¹A¹ÜæŖŹ¼·“Ó¦£¬ŌŚB¹ÜÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ____________Š“³öBÖŠ·¢Éś·“Ó¦µÄĖłÓŠĄė×Ó·½³ĢŹ½£ŗ___________________
¢ŚĶ¬Ń§ŅŅ£ŗ“ņæŖa£¬Ź¹A¹ÜÖŠ·“Ó¦Ņ»¶ĪŹ±¼äŌŁ¼Š½ōÖ¹Ė®¼Ša£¬ŹµŃéÖŠŌŚB¹ÜÖŠ¹Ū²ģµ½µÄĻÖĻóŹĒ__________ £»
¢ŪĶ¬Ń§ŅŅ“ņæŖaµÄÄæµÄ______________£¬øł¾ŻŅŌÉĻŹµŃéÅŠ¶Ļ___________£ØĢī¼×»ņŅŅ£©Ķ¬Ń§æɳɹ¦”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ298.15KŹ±£¬æÉÄę·“Ó¦:Pb2+£Øaq£©+Sn£Øs£©![]() Pb£Øs£©+Sn2+£Øaq£©µÄĘ½ŗā³£ŹżK=2.2£¬ČōČÜŅŗÖŠPb2+ŗĶSn2+µÄÅØ¶Č¾łĪŖ0.010mol”¤L-1£¬Ōņ·“Ó¦½ųŠŠµÄ·½ĻņŹĒ
Pb£Øs£©+Sn2+£Øaq£©µÄĘ½ŗā³£ŹżK=2.2£¬ČōČÜŅŗÖŠPb2+ŗĶSn2+µÄÅØ¶Č¾łĪŖ0.010mol”¤L-1£¬Ōņ·“Ó¦½ųŠŠµÄ·½ĻņŹĒ
A. ĻņÓŅ½ųŠŠ B. Ļņ×ó½ųŠŠ C. “¦ÓŚĘ½ŗāדĢ¬ D. ĪŽ·ØÅŠ¶Ļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×“¼ŹĒÖŲŅŖµÄ»Æѧ¹¤Ņµ»ł“”ŌĮĻŗĶĒå½ąŅŗĢåČ¼ĮĻ”£ŅŃÖŖÖʱø¼×“¼µÄÓŠ¹Ų»Æѧ·“Ó¦ŅŌ¼°ŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄ»Æѧ·“Ó¦Ę½ŗā³£ŹżČēĻĀ±ķĖłŹ¾£ŗ
»Æѧ·“Ó¦ | Ę½ŗā³£Źż | ĪĀ¶Č/”ę | |
500 | 800 | ||
¢Ł2H2(g)£«CO(g) | K1 | 2.5 | 0.15 |
¢ŚH2(g)£«CO2(g) | K2 | 1.0 | 2.50 |
¢Ū3H2(g)£«CO2(g) | K3 | ||
£Ø1£©¾Ż·“Ó¦¢ŁÓė¢ŚæÉĶʵ¼³öK1”¢K2ÓėK3Ö®¼äµÄ¹ŲĻµ£¬ŌņK3£½________(ÓĆK1”¢K2±ķŹ¾)”£
£Ø2£©·“Ó¦¢ŪµÄ¦¤H_________0(Ģī”°£¾”±»ņ”°£¼”±)”£
£Ø3£©500”ꏱ²āµĆ·“Ó¦¢ŪŌŚÄ³Ź±æĢH2(g)”¢CO2(g)”¢CH3OH(g)”¢H2O(g)µÄÅضČ(mol”¤L£1)·Ö±šĪŖ0.8”¢0.1”¢0.3”¢0.15£¬Ōņ“ĖŹ±¦ŌÕż_____¦ŌÄę(Ģī”°>”±”¢”°£½”±»ņ”°<”±)”£
£Ø4£©500”ꏱ2LĆܱÕČŻĘ÷ÖŠĶ¶Čėa mol H2”¢b mol CO·¢Éś·“Ó¦¢Ł£»²āµĆĘ½ŗāŹ±H2(g)”¢CO(g)µÄÅضČ(mol”¤L£1)·Ö±šĪŖ0.2”¢0.1Ōņ£ŗ
¢ŁĘ½ŗāŹ±H2µÄ×Ŗ»ÆĀŹĪŖ________£Ø±£ĮōŅ»Ī»ÓŠŠ§Źż×Ö£©”£
¢ŚČōĻņĘ½ŗāŗóµÄČŻĘ÷ÖŠŌŁĶ¶Čėa mol H2”¢b mol CO£¬“ļĘ½ŗāŗó£¬CH3OHµÄĢå»ż·ÖŹżÓėŌĘ½ŗāĻą±Č______________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌĻĀĮŠĢ½¾æ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲµÄĖÄøöŹµŃ飬»Ų“šĻĀĮŠĪŹĢā£ŗ
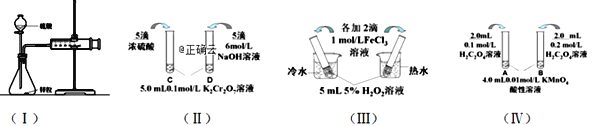
£Ø1£©ĄūÓĆŹµŃé£Ø¢ń£©Ģ½¾æŠæÓė1mol/LĮņĖįŗĶ4mol/LĮņĖį·“Ó¦µÄĖŁĀŹ£¬æÉŅŌ²ā¶ØŹÕ¼ÆŅ»¶ØĢå»żĒāĘųĖłÓƵď±¼ä”£“Ė·½·ØŠčŅŖæŲÖʵıäĮæÓŠ£ØÖĮÉŁŠ“³öĮ½Ļī£©£ŗ______________________”£
£Ø2£©ŹµŃé£Ø¢ņ£©ŅŃÖŖ£ŗCr2O72- £Ø³ČÉ«£©+ H2O![]() 2CrO42- £Ø»ĘÉ«£©+ 2H+”£DŹŌ¹ÜÖŠŹµŃéĻÖĻóĪŖ______________£¬ÓĆĘ½ŗāŅʶÆŌĄķ½āŹĶŌŅņ£ŗ_______________
2CrO42- £Ø»ĘÉ«£©+ 2H+”£DŹŌ¹ÜÖŠŹµŃéĻÖĻóĪŖ______________£¬ÓĆĘ½ŗāŅʶÆŌĄķ½āŹĶŌŅņ£ŗ_______________
£Ø3£©ŹµŃé£Ø¢ó£©ÖŠŹµŃéÄæµÄŹĒĢ½¾æ____________________”£
£Ø4£©ŌŚŹŅĪĀĻĀ½ųŠŠŹµŃé£Ø¢ō£©ČÜŅŗĶŹÉ«µÄŹ±¼ä£ŗt(A)________t(B)£ØĢī>”¢<»ņ= £©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com