
【题目】1LMgSO4和CuSO4的混合液中c(SO42-)= 2mol/L,用石墨电极电解此溶液,通电一段时间,两极上均产生22.4L(标准状况)气体,则原混合液中Mg2+的浓度是( )
A. 0.5mol/L B. 1mol/L C. 1.5mol/L D. 2mol/L
【答案】B
【解析】n(气体)=![]() =1mol。阳极电极反应式为:4OH--4e-=O2↑+2H2O,n(O2)=1mol,则电路中通过的电子物质的量为4mol;阴极产生气体的电极反应式为:2H++2e-=H2↑,n(H2)=1mol,生成H2得到电子物质的量为2mol;则阴极上Cu2+放电得到电子物质的量为4mol-2mol=2mol,根据Cu2++2e-=Cu,n(Cu2+)=1mol,c(Cu2+)=1mol
=1mol。阳极电极反应式为:4OH--4e-=O2↑+2H2O,n(O2)=1mol,则电路中通过的电子物质的量为4mol;阴极产生气体的电极反应式为:2H++2e-=H2↑,n(H2)=1mol,生成H2得到电子物质的量为2mol;则阴极上Cu2+放电得到电子物质的量为4mol-2mol=2mol,根据Cu2++2e-=Cu,n(Cu2+)=1mol,c(Cu2+)=1mol![]() 1L=1mol/L;根据电荷守恒:2c(Mg2+)+2c(Cu2+)=2c(SO42-),c(Mg2+)=(2mol/L
1L=1mol/L;根据电荷守恒:2c(Mg2+)+2c(Cu2+)=2c(SO42-),c(Mg2+)=(2mol/L![]() 2-1mol/L
2-1mol/L![]() 2)
2)![]() 2=1mol/L,答案选B。
2=1mol/L,答案选B。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】秸秆(含多糖物质)的综合应用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
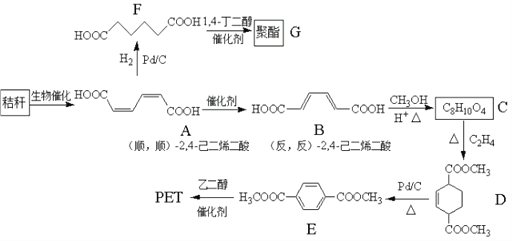
回答下列问题:
(1)下列关于糖类的说法正确的是______________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为______。
(3)D中官能团名称为______,D生成E的反应类型为______。
(4)F 的化学名称是______,由F生成G的化学方程式为______。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成44 gCO2,W共有______种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为_________。
(6)参照上述合成路线,以(反,反)-2,4-己二烯和C2H4为原料(无机试剂任选),设计制备对二苯二甲酸的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.5g铁铝混合物粉末加入过量的1L1mol/L HNO3溶液中,充分反应后,得3.36L(标准状况)NO气体,求
(1)假设反应前后溶液的体积不变,剩余硝酸的浓度为mol/L
(2)混合物中铝的质量分数为%,
(3)向反应后的溶液中加入mL 1mol/L NaOH溶液时,生成的沉淀量最大,再加mL 1mol/L NaOH溶液才能使沉淀的量不再发生变化.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁﹣次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO—+H2O═Mg(OH)2+Cl—下列有关说法正确的是( )

A. 电池工作时,C溶液中的溶质是MgCl2
B. 负极反应式:ClO—﹣2e—+H2O═Cl—+2 OH—
C. 每转移0.1mol电子,理论上生成0.1mol Cl—
D. 电池工作时,正极a附近的pH将不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. MgO(s)+C(s)=Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H<0
B. 0.1mol/L的CH3COONa溶液加水稀释后,溶液中![]() 的值减小
的值减小
C. 常温常压下,4.4gCO2与足量Na2O2完全反应生成O2分子数为6.02×1022个
D. 用pH均为2的盐酸和甲酸中和等物质的量的NaOH溶液,盐酸消耗的体积多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 新制饱和氯水中:A13+、Cu2+、SO42-、Br-
B. 甲基橙变红的溶液:Mg2+、Fe2+、NO3-、SCN-
C.  的溶液中:Na+、K+、Cl-、AlO2-
的溶液中:Na+、K+、Cl-、AlO2-
D. 水电离的c(H+)=1×10-13mol/L的溶液中:Ca2+、Ba2+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石棉尾矿主要含有Mg3(Si2O5)(OH)4和少量的Fe2O3、Al2O3 . 以石棉尾矿为供源制备碳酸镁晶须(MgCO3nH2O)的工艺如下: 
已知“焙烧”过程中的主反应为:
Mg3(Si2O5)(OH)4+5(NH4)2SO4 3Mg ![]() SO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
SO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)写出焙烧产物NH3的电子式 .
(2)为提高水浸速率,可采取的措施为(任写一条).“浸渣”的主要成分为 .
(3)“除铁、铝”时,需将pH调至8.0左右,适宜作调节剂的是(填字母代号). a.NaOH Ca(OH)2 c.NH3H2O
(4)“沉镁”过程中反应的离子方程式为 .
(5)流程中可以循环利用的物质是(填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性气体电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法正确的是

A. a极与电源的负极相连
B. 产物丁为硫酸溶液
C. 离子交换膜d为阴离子交换膜(允许阴离子通过)
D. b电极反立式为2H2O+2e-=2OH-+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com