
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
���� ����NaOH+CO2=NaHCO3��NaHCO3+NaOH=Na2CO3+H2O֪����NaOH��Һ��CO2����ȡ��Na2CO3��Һ�����������̼����������NaHCO3�����������̼������������Һ���״�������NaOH��Ϊ����ȡ�ϴ�����Na2CO3��Һ��Ӧ����ȡ������ͬ�������ͬŨ�ȵ�NaOH��Һ��������һ����ͨ�����������̼��ȡNaHCO3��Ȼ����ȡ��NaHCO3��Һ������һ��NaOH��Һ�м��ɵõ��ϴ�����Na2CO3��Һ���ݴ˷������
��� �⣺����NaOH+CO2=NaHCO3��NaHCO3+NaOH=Na2CO3+H2O֪����NaOH��Һ��CO2����ȡ��Na2CO3��Һ�����������̼����������NaHCO3�����������̼������������Һ���״�������NaOH��Ϊ����ȡ�ϴ�����Na2CO3��Һ��Ӧ����ȡ������ͬ�������ͬŨ�ȵ�NaOH��Һ��������һ����ͨ�����������̼��ȡNaHCO3��Ȼ����ȡ��NaHCO3��Һ������һ��NaOH��Һ�м��ɵõ��ϴ�����Na2CO3��Һ��
��1������ʵ����Ҫ��ȡ������̼����ȡ������̼ʱ��Ҫ���շ���������Ƥ�ܡ��������ܣ�����Ҫ�ձ�ʢ������������Һ����Ͳ��ȡ��Һ���ʴ�Ϊ���ձ�����Ͳ��
��2��ʵ��ʱ��Ҫ��ȡ̼��������Һ����ȡ̼��������Һʱ������ҪNaOH��Һ���Ҫ������̼��ʵ������ϡ����ʹ���ʯ�Ʊ�������̼����ѡ�ܢݣ��ʴ�Ϊ���ܢݣ�
��3�����ݷ���֪�����������Ϊ������ȡһ������NaOH��Һ�ֳ����ȷݣ�
����ȡCO2��������һ��NaOH��Һ��ͨ�˹�����CO2���壬
�۽�������Һ���ҡ�ȣ�
�ʴ�Ϊ������ȡһ������NaOH��Һ�ֳ����ȷݣ�
����ȡCO2��������һ��NaOH��Һ��ͨ�˹�����CO2���壬
�۽�������Һ���ҡ�ȣ�
��4���ӱ��п�֪��NaHCO3�������ܽ��Ϊ8.4g���賣�����ܽ��NaOH������Ϊxʱ��NaHCO3�ﵽ���ͣ�
NaOH+CO2=NaHCO3
40 84
x 8.4g
x=4g
����Һ��NaOH��������������$\frac{4g}{100g+4g}$��100%=3.85%ʱ���ڲ��������NaHCO3����������
���� ���⿼�������Ʊ�ʵ�鷽����ƣ��漰̼���ƺ�̼�����Ƶ����ʣ����ؿ���ѧ��ʵ�����������֪ʶ������������ȷʵ��ԭ���ǽⱾ��ؼ������ʵ��Ŀ�����ʵ�飬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Fe3+ | Fe2+ | Cu2+ | |
| �������↑ʼ����ʱ��pH | 1.9 | 7 | 4.7 |
| �������������ȫʱ��pH | 3.2 | 9 | 6.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
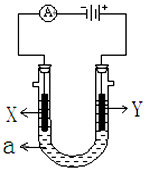 ��ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
��ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͬ����������� | B�� | ����ͬ������������ | ||
| C�� | ������ͬ������������ | D�� | ����ͬ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ���ҿ����ű���ʳ��ˮ�ķ����ռ����� | |
| B�� | �Ӵ�����ʹN2��H2��һ��������ת��ΪNH3 | |
| C�� | ����ˮƿ�������д����������ݳ� | |
| D�� | Fe��SCN��3��Һ�м���6mol/LNaOH��Һ����ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
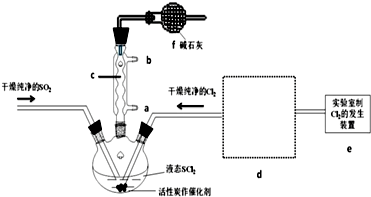
| ���� | �� | �� | �� | �� |
| ����װ�� | 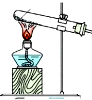 | 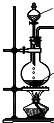 | 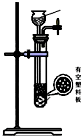 | 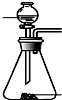 |
| ��ѡ�Լ� | NaHSO3���� | 18.4mol/LH2SO4 | 4mol/LHNO3+NaHSO3 | 70%NaHSO4+K2SO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| Ԫ�ر�� | Ԫ��������Ϣ |
| A | �䵥�����ܶ���С������ |
| B | �����Ӵ�������λ����ɣ������ǿ�������Ҫ�ɷ�֮һ |
| C | ����������B������������ͬ�ĵ��Ӳ�ṹ������B�����γ��������ӻ����� |
| D | ����������������ﶼ�����ԣ���Cͬ���� |
| E | ��Cͬ���ڣ�ԭ�Ӱ뾶�ڸ�������С |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
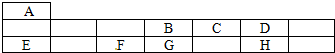
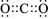 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
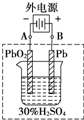 Ǧ�����ǵ��͵Ŀɳ���أ����������������Ƕ��Բ��ϣ���ش��������⣨�������⡢����������ԭ����
Ǧ�����ǵ��͵Ŀɳ���أ����������������Ƕ��Բ��ϣ���ش��������⣨�������⡢����������ԭ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com