
【题目】高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K= ![]() ,已知1100℃时K=0.263
,已知1100℃时K=0.263
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值;平衡常数K值(选填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025molL﹣1、c(CO)=0.1molL﹣1 , 在这种情况下,该反应是否处于化学平衡状态(选填“是”或“否”),此时,化学反应速率是v(正)v(逆)(选填“大于”“小于”或“等于”),其原因是 .
【答案】
(1)增大;增大
(2)否;大于;Qc= ![]() =0.25<0.263,因为温度不变,K不变,为增大K平衡应向正向移动,所以v(正)>v(逆)
=0.25<0.263,因为温度不变,K不变,为增大K平衡应向正向移动,所以v(正)>v(逆)
【解析】解:(1)可逆反应FeO(s)+CO (g)Fe(s)+CO2(g)的平衡常数表达式k= ![]() ;该反应正反应是放热反应,温度降低平衡向正反应方向移动,CO2的物质的量增大、CO的物质的量减小,故到达新平衡是CO2与CO的体积之比增大,其平衡常数增大,所以答案是:增大;增大;(2)此时浓度商Qc=
;该反应正反应是放热反应,温度降低平衡向正反应方向移动,CO2的物质的量增大、CO的物质的量减小,故到达新平衡是CO2与CO的体积之比增大,其平衡常数增大,所以答案是:增大;增大;(2)此时浓度商Qc= ![]() =0.25,小于平衡常数0.263,故反应不是平衡状态,反应向正反应方向进行,v(正)>v(逆),所以答案是:否;大于;Qc=
=0.25,小于平衡常数0.263,故反应不是平衡状态,反应向正反应方向进行,v(正)>v(逆),所以答案是:否;大于;Qc= ![]() =0.25<0.263,因为温度不变,K不变,为增大K平衡应向正向移动,所以v(正)>v(逆).
=0.25<0.263,因为温度不变,K不变,为增大K平衡应向正向移动,所以v(正)>v(逆).
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( ) 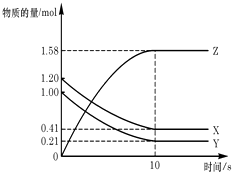
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若3.01×1023个气体分子在某状况下的体积为22.4L,则该状况下的气体摩尔体积为
A. 11.2L/mol B. 22.4L/mol C. 44.8L/mol D. 67.2L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E,F为原子序数依次增大的短周期主族元素.A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级且每个能级上的电子数相同;A与C形成的分子为三角锥形;D原子p轨道上成对的电子总数等于未成对的电子总数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F.
(1)A,C形成的分子极易溶于水,与该分子互为等电子体的阳离子为 .
(2)比较E、F的第一电离能:E(填“>”或“<”)F.
(3)BD2在高温高压下所形成的晶胞如图所示.该晶体的类型属于(填“分子”“原子”“离子”或“金属”)晶体,该晶体中B原子的杂化形式为 . 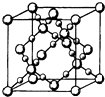
(4)单质F与强碱溶液反应有[F(OH)4]﹣生成,则[F(OH)4]﹣中存在(填字母). a.共价键 b.非极性键 c.配位键 d.σ键 e.π键
(5)Cu晶体是面心立方体,立方体的每个面5个Cu原子紧密堆砌,已知每个Cu原子的质量为a g,Cu原子半径为d cm,求该晶体的密度为gcm﹣3 . (用含a、d的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.从溶液中结晶出来的晶体都含结晶水
B.晶体失去结晶水一定是风化的结杲
C.风化与潮解是两个正好相反的过程
D.某饱和溶液冷却析出晶体后,该溶液仍是饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中进行如下反应:CO(g)+H2O(g)CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是( )
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K= ![]()
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照要求填空:
(1)下面列出了几组物质,请将物质的合适组号填写在空格上. 同位素 , 同素异形体 , 同分异构体 , 同系物 .
①金刚石与“足球烯”C60;②D与T;③16O、17O和18O;④氧气(O2)与臭氧(O3);
⑤ 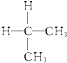 与
与 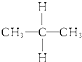 ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
⑦ ![]() 和
和 ![]() ;⑧
;⑧ ![]() 和
和 ![]() ;
;
(2)完成离子方程式:MnO4﹣+C2O42﹣+=Mn2++CO2↑+
(3)命名有机物: ![]()
(4)写出乙酸与甲醇(CH3OH)酯化的化学方程式 .
(5)将铂丝插入KOH溶液中做电极,并在两极片上分别通入甲烷和氧气,形成一种燃料电池:通甲烷的铂丝为原电池的极,发生的电极反应为 .
(6)PET是涤纶的主要成分,可用作饮料瓶、磁带和胶片的片基等,其结构简式如图: ![]() .该高分子材料是由两种单体通过缩聚反应制备而成,其单体的结构简式为和 .
.该高分子材料是由两种单体通过缩聚反应制备而成,其单体的结构简式为和 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com