
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成RB2型常见化合物,并知在DB2和EB2中,D与B的质量比为7:8,E与B的质量比为1:1.根据以上条件,回答下列问题:
(1)写出下列元素(用元素符号回答):C ,D ,E .
(2)写出D原子的电子排布式 .
(3)写出工业上由单质A制取单质D的化学方程式 .
(4)指出E元素在元素周期表中的位置 .
(5)比较A、B、C三种元素的第一电离能的大小顺序 (按由大到小的顺序排列,用元素符号表示).
(6)比较元素D和E的电负性的相对大小(用元素符号表示) .
考点:
位置结构性质的相互关系应用.
专题:
元素周期律与元素周期表专题.
分析:
p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,依据常见化合物可推断B为氧元素,C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×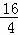 =28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,结合元素对应原子的结构、单质以及化合物的性质解答该题.
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,结合元素对应原子的结构、单质以及化合物的性质解答该题.
解答:
解:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,则A的核外电子排布为1s22s22p2,应为C元素,B元素可分别与A、C、D、E生成RB2型化合物,且A、B、C属于同一周期,依据常见化合物可推断B为氧元素,C为N元素,可形成NO2化合物,在DB2和EB2中,D与B的质量比为7:8,则有M(D):M(O)=7:4,M(D)=7×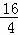 =28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,
=28,D应为Si元素;E与B的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,
综上所述:A为碳、B为氧、C为氮、D为硅、E为硫,
(1)C为氮、D为硅、E为硫,元素符号分别为:N、Si、S,故答案为:N;Si;S;
(2)D为Si,Si元素为14号元素,原子核外有14个电子,所以核外电子排布式为:1s22s22p63s23p2,故答案为:1s22s22p63s23p2;
(3)C与二氧化硅反应生成硅单质与一氧化碳,化学反应方程式为:SiO2+2C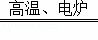 Si+2CO↑,故答案为:SiO2+2C
Si+2CO↑,故答案为:SiO2+2C Si+2CO↑;
Si+2CO↑;
(4)E元素为S,S有16个质子,处于第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(5)元素的非金属性越强,其第一电离能越大,但是由于N元素的p轨道处于半充满状态,故N的第一电离能大于O,故答案为:N>O>C;
(6)元素的非金属性越强,其电负性越大,由于非金属性S大于Si,故电负性S>Si,故答案为:S.
点评:
本题主要考查的是元素的推断以及元素化合物的知识,充分利用题给信息,准确推断出各种元素是解决本题的关键,属于常考题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列各组中每种物质都既有离子键又有共价键的一组是()
A. NaOH、H2SO4、(NH4)2SO4 B. MgO、Na2SO4、HNO3
C. Na2O2、KOH、Na3PO4 D. HCl、Fe2O3、MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
3Cl2+8NH3=6NH4Cl+N2的反应中,被氧化的NH3与未被氧化的NH3的分子数之比为()
A. 1:6 B. 3:1 C. 1:3 D. 6:1
查看答案和解析>>
科目:高中化学 来源: 题型:
氢原子的电子云图中的小黑点表示的意义是( )
|
| A. | 一个黑点表示一个电子 |
|
| B. | 黑点的多少表示电子个数的多少 |
|
| C. | 表示电子运动的轨迹 |
|
| D. | 电子在核外空间出现机会的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
国际通用的元素符号是用1个或2个拉丁文字母表示的,其中第一个字母大写,第二个字母小写.镍元素的拉丁文名称为Niccolum,则镍的元素符号为( )
|
| A. | Ni | B. | NI | C. | N | D. | Na |
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表中,同周期元素的结构和性质呈现一定的规律性变化.下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出).下列有关说法不正确的是( )
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10﹣10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 | +2 | ④ | +4 ﹣4 | +5 ﹣3 | ⑤ | +7 ﹣1 |
|
| A. | ⑤处的最高正价是+6,最低负价是﹣2 |
|
| B. | ③处的数值介于1.10﹣1.43之间 |
|
| C. | 第三周期元素(Na﹣Cl)的最高正价数等于其原子的最外层电子数 |
|
| D. | 元素①的原子序数是13,①和②形成的化合物的化学式为AlS |
查看答案和解析>>
科目:高中化学 来源: 题型:
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是()
A. 利用电池外壳的金属材料
B. 防止电池中汞、镉和铅等重金属离子对土壤和水源造成污染
C. 不使电池中渗透的电解液腐蚀其他物品
D. 回收其中石墨电极
查看答案和解析>>
科目:高中化学 来源: 题型:
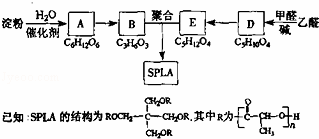
星形聚合物SPLA可经下列反应路线得到(部分反应条件未注明).
(1)淀粉是多糖(填“单”或“多”);A的名称是葡萄糖.
(2)乙醛由不饱和烃制备的方法之一是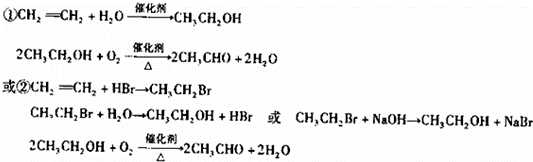 (用化学方程式表示,可多步).
(用化学方程式表示,可多步).
(3)D→E的化学反应类型属于 反应;D结构中有3个相同的基团,且1molD能与2molAg(NH3)2OH反应,则D的结构简式是 ;D与银氨溶液反应的化学方程式为 .
(4)B的直链同分异构体G的分子中不含甲基,G既不能与NaHCO3溶液反应,又不能与新制Cu(OH)2反应,且1molG与足量Na反应生成1mol H2,则G的结构简式为 .
(5)B有多种脱水产物,其中两种产物的结构简式为 和 (写两种即可).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com