
| A. | 过滤时,玻璃棒与三层滤纸的一边接触 | |
| B. | 过滤时,漏斗下端紧贴烧杯内壁 | |
| C. | 分液时,上层液体要从分液漏斗上口倒出 | |
| D. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 |
分析 A.为了避免玻璃杯将滤纸损坏,应该将玻璃杯与三层滤纸的一边接触;
B.过滤时,为了避免滤液溅出,漏斗下端紧贴烧杯内壁;
C.为了避免污染试剂,上层液体要从分液漏斗上口倒出,下层液体从分液漏斗的下端放出;
D.向试管内滴加液体时胶头滴管应竖直悬空.
解答 解:A.过滤操作时,避免玻璃杯损坏滤纸,需要将玻璃棒与三层滤纸的一边接触,故A正确;
B.过滤操作时漏斗下端紧靠在烧杯内壁可以防止液滴溅出,故B正确;
C.分液操作时,避免试剂被污染,上层液体需要从分液漏斗上口倒出,故C正确;
D.向试管内滴加液体时胶头滴管应竖直悬空,不能紧贴试管内壁,否则易污染试剂,故D错误;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及过滤、分液、胶头滴管的使用方法等知识,明确化学实验基本操作方法为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | (1)(3)(5) | B. | (1)(3)(4) | C. | (1)(2)(4)(5) | D. | (1)(2)(3)(4)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠可用作潜艇里氧气的来源 | B. | 二氧化硅是制造光电池的原料 | ||
| C. | 氯气可用于制造漂白粉 | D. | 硅酸钠溶液可用作木材防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加氢氧化钠溶液,加热,滴入酚酞试剂 | |
| B. | 加水,将湿润的红色石蕊试纸放在试管口 | |
| C. | 加氢氧化钠溶液,加热,滴入紫色石蕊试剂 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
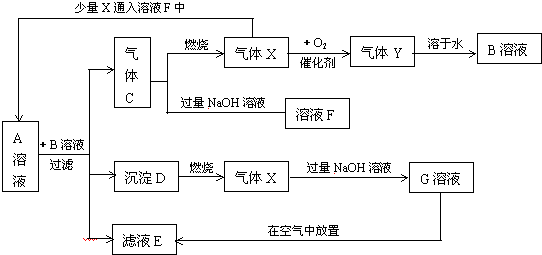
| A. | 气体C是SO2 | |
| B. | 溶液A和溶液B可能的化学反应为3Na2S+Na2SO3+4H2SO4=3S↓+H2S↑+4Na2SO4+3H2O | |
| C. | 若氧气足量气体C可以一步反应得到气体Y | |
| D. | 图中少量X通入溶液F中不涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
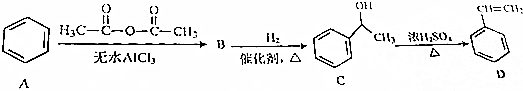
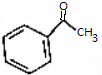 .
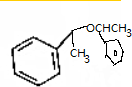
.
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com