
| A. | 单质的熔沸点逐渐降低 | B. | 卤素原子半径逐浙减少 | ||
| C. | 最高正化合价逐渐增大 | D. | 单质的氧化性逐渐减弱 |
分析 A.卤素单质都是分子晶体,其熔沸点随着相对分子质量增大而增大;
B.原子电子层数越多其原子半径越大;
C.主族元素中,其最高正化合价与其族序数相等,但O、F元素没有正化合价;
D.元素的非金属性越强,其单质的氧化性越强.
解答 解:A.卤素单质都是分子晶体,其熔沸点随着相对分子质量增大而增大,卤族元素中随着原子序数增大其分子的相对分子质量增大,所以其熔沸点逐渐升高,故A错误;
B.原子电子层数越多其原子半径越大,随着原子序数增大其电子层数逐渐增多,所以原子半径逐渐增大,故B错误;
C.主族元素中,其最高正化合价与其族序数相等,但O、F元素没有正化合价,卤族元素中其最高正化合价都是+7(F元素除外),故C错误;
D.元素的非金属性越强,其单质的氧化性越强,卤族元素中,随着原子序数增大元素非金属性逐渐减弱,所以其单质的氧化性逐渐减弱,故D正确;
故选D.
点评 本题考查同一主族元素性质递变规律,为高考高频点,熟练掌握碱金属族、卤族元素及第三周期元素原子结构及其性质递变规律,注意规律中的特殊现象,易错选项是C.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②③④⑤⑥ | C. | ④⑤⑥⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中C、H、O的个数比为1:2:3 | B. | 分子中C、H的个数比为1:2 | ||
| C. | 该有机物的相对分子质量为14 | D. | 该分子中肯定不含氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现需90mL1.0mol/LNaOH溶液,称取3.6gNaOH固体配制--溶液浓度偏低 | |
| B. | 测定溶液 pH的实验中,用润湿的pH试纸测定新制氯水的pH--测定结果偏高 | |
| C. | 中和热实验测定中,缓慢地将NaOH溶液倒入测定装置中--对测定结果无影响 | |
| D. | 酸碱中和滴定实验中,标准液滴定前无气泡而滴定后有气泡--测定结果偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  装置中阳极上析出红色固体 | |
| B. |  装置的待镀铁制品应与电源负极相连 | |
| C. |  装置中粗铜应与电源负极相连 | |
| D. | 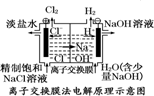 装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
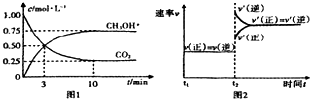
| A. | 平衡时该反应的平衡常数=$\frac{16}{3}(mol/L)^{-2}$ | |
| B. | 平衡时CO2的转化率为50% | |
| C. | t2时刻改变的条件是高温度 | |
| D. | 在0-3min时H2的反应速率为0.5mol•(L•min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液 Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2 H2O | |
| B. | 碳酸钠溶液与醋酸反应 CO32-+2H+=CO2↑+H2O | |
| C. | Ca (ClO)2溶液中通入过量的二氧化硫气体 ClO-+H2O+SO2=HSO3-+HClO | |
| D. | 硫化氢气体通入硫酸铁溶液中:H2S+2Fe3+=2Fe2++S↓+2H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com