
| A. | 三氯化硼液态时能导电而固态时不导电 | |
| B. | 三氯化硼加到水中使溶液的pH升高 | |
| C. | 三氯化硼分子呈正三角形,属非极性分子 | |
| D. | 分子中所有原子都满足最外层8电子稳定结构 |
分析 A.氯化硼是共价化合物;
B.三氯化硼水解生成HCl;
C.三氯化硼中的硼为sp2杂化,无孤对电子;
D.原子的价电子数加上化合价的绝对值等于8,则为8电子稳定结构.
解答 解:A.氯化硼是共价化合物液态时不能导电,故A错误;
B.三氯化硼加到水中会发生水解生成HCl,则使溶液的pH降低,故B错误;
C.三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构,为非极性分子,故C正确;
D.三氯化硼中B的价电子数为3,化合价为+3,则分子中B的最外层电子数为3+3=6,则B不满足最外层8电子稳定结构,故D错误.
故选C.
点评 本题考查原子轨道杂化、分子立体构型、8电子稳定结构等,难度适中,注意三氯化硼中的硼为sp2杂化,无孤对电子,分子中键与键之间的夹角为120°,是平面三角形结构.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
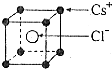
| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$ | B. | $\frac{6M}{{N}_{A}•{a}^{3}}$ | C. | $\frac{4M}{{N}_{A}•{a}^{3}}$ | D. | $\frac{M}{{N}_{A}•{a}^{3}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H16与甲烷互为同系物 | |
| B. | 乙烯只能加成、不能取代,苯只能取代、不能加成 | |
| C. | CH3CH2CH2CH3和 互为同分异构体 互为同分异构体 | |
| D. |  和 和 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
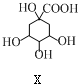 $→_{一定条件}^{Y}$
$→_{一定条件}^{Y}$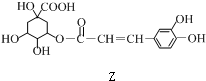
| A. | X分别与足量的Na、NaOH反应,消耗两者的物质的量之比为5﹕1 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1 mol Z与浓溴水反应最多消耗4molBr2 | |
| D. | 1 mol Z与足量NaOH溶液反应,最多消耗4mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 吸氢材料镧镍合金 | B. | 半导体材料砷化镓 | ||
| C. | 高温结构陶瓷材料氮化硅 | D. | 透明陶瓷材料硒化锌 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
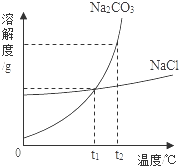 我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:
我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com