
| A. | 非金属氧化物都是酸性氧化物 | |
| B. | 凡是酸性氧化物都可以直接与水反应生成对应的酸 | |
| C. | 氧化物都能与酸或碱反应生成盐 | |
| D. | 碱性氧化物都是金属氧化物 |
分析 A、非金属氧化物不一定是酸性氧化物;
B、酸性氧化物不一定和水反应得到对应的酸;
C、氧化物不一定都能与酸或碱反应生成盐,有的氧化物属于不成盐氧化物;
D、碱性氧化物都是金属氧化物.
解答 解:A、非金属氧化物不一定是酸性氧化物,如CO、NO属于不成盐氧化物,故A错误;
B、酸性氧化物不一定和水反应得到对应的酸,如二氧化硅和水之间不反应,故B错误;
C、氧化物不一定都能与酸或碱反应生成盐,有的氧化物属于不成盐氧化物,如CO、NO,故C错误;
D、碱性氧化物可以和酸之间反应生成盐和水,所有的碱性氧化物都是金属氧化物,故D正确.
故选D.
点评 本题考查了酸性氧化物与非金属氧化物、碱性氧化物与金属氧化物之间的辩证关系,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 3.20g | B. | 10.22g | C. | 12.62g | D. | 13.70g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 各物质的浓度之比c(A):c(B):c(C)=2:3:4 | |
| B. | 混合气体中各物质的浓度相等 | |
| C. | 单位时间内,若消耗了a molA物质,同时也消耗了2a mol C物质 | |
| D. | 混合气体的体积是反应开始前的$\frac{4}{5}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2比O3质量小 | B. | 两气体分子数目相等 | ||
| C. | 两气体的压强相等 | D. | 两气体的氧原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③②① | B. | ②①③ | C. | ①②③ | D. | ③①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| D. | 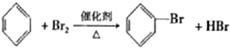 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯是发生取代反应 | |
| B. | C5H10不属于烷烃,C5H12属于烷烃且有三种同分异构体 | |
| C. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 | |
| D. | 乙酸、葡萄糖在一定条件下均能与Cu(OH)2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ki1的表达式为Ki1=$\frac{[{H}_{2}C{O}_{3}]}{[{H}^{+}][HC{{O}_{3}}^{-}]}$ | |
| B. | Ki2对应的电离过程是HCO3-+H2O?H3O++CO32- | |
| C. | 当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 | |
| D. | 改变条件使Ki1减小,则Ki2一定也减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com