
分析 (1)结合c(OH-)=$\sqrt{\frac{Ksp}{c(M{g}^{2+})}}$计算;
(2)A.氯化铵中铵根离子水解显碱性;
B.醋酸与一水合氨的电离平衡常数相等;
C.将饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,可看到白色沉淀溶解.产生这种现象的原因存在以下两种观点.
观点①:2NH4++Mg(OH)2═2NH3•H2O+Mg2+;
观点②为铵根离子水解生成的氢离子与氢氧化镁反应,可利用醋酸铵代替NH4Cl溶液作对照实验说明.
解答 解:(1)当溶液中c(Mg2+)≤1.0×10-5mol/L可视为沉淀完全,则此温度下应保持溶液中c(OH-)≥$\sqrt{\frac{6.4×10-12}{1×1{0}^{-5}}}$=8×10-4mol•L-1,故答案为:8×10-4;
(2)A..氯化铵中铵根离子水解显碱性,发生水解离子反应为NH4++H2O?NH3•H2O+H+,离子浓度为 c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:NH4++H2O?NH3•H2O+H+;c(Cl-)>c(NH4+)>c(H+)>c(OH-);
B.醋酸与一水合氨的电离平衡常数相等,则CH3COONH4溶液显中性,故答案为:中;
C.观点②的离子方程式为NH4++H2O?NH3•H2O+H+、Mg(OH)2+2H+=Mg2++2H2O;利用醋酸铵代替NH4Cl溶液作对照实验说明,若仍溶液可知观点①成立,反应②成立,
故答案为:NH4++H2O?NH3•H2O+H+、Mg(OH)2+2H+=Mg2++2H2O;c.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握Ksp的计算、盐类水解、平衡移动为解答的关键,侧重分析与应用能力的考查,注意溶解平衡移动的实验探究,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.025 mol/L | B. | 0.30mol/L | C. | 0.36mol/L | D. | 0.45mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | n (CO)/mol | n (Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.20 | |
| 4 | 0.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
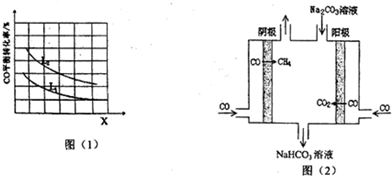
 向大气中排放过量的二氧化碳是造成全球气候变暖的重要因素,所以二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.
向大气中排放过量的二氧化碳是造成全球气候变暖的重要因素,所以二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向. ;将足量的C02通入下列溶液中,最终溶液变浑浊的是ce.
;将足量的C02通入下列溶液中,最终溶液变浑浊的是ce.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶可用作加热的反应器 | |
| B. | 室温下,不能将浓硫酸盛放在铁桶中 | |
| C. | 在50mL量筒中配置0.1000mol•L-1碳酸钠溶液 | |
| D. | 用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com