
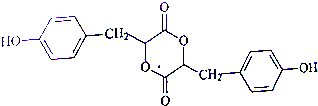
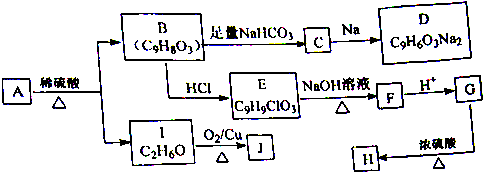
 .
.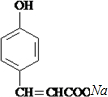 +
+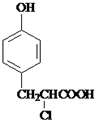 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +HCl.
+HCl. 分析 由信息①知,A分子含有酚羟基,两个取代基在苯环的对位;I催化氧化生成J,J能发生银镜反应,则I为CH3CH2OH、J为CH3CHO;A在浓硫酸作用下进行酯的水解反应生成B和I,根据B的分子式可知,B的不饱和度为$\frac{9×2+2-8}{2}$=6,苯环和1个羧基的不饱和度为:4+1=5,说明B的侧链中还含有1个碳碳双键,则B为 、A为
、A为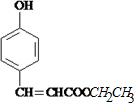 ;B与HCl发生加成反应生成E,则E为
;B与HCl发生加成反应生成E,则E为 ;E与氢氧化钠溶液加热反应生成F,则F为
;E与氢氧化钠溶液加热反应生成F,则F为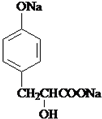 ,F在酸性条件下转化成G,则G为
,F在酸性条件下转化成G,则G为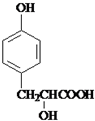 ;两分子G之间发生酯化反应生成H;B与碳酸氢钠反应生成C,则C为
;两分子G之间发生酯化反应生成H;B与碳酸氢钠反应生成C,则C为 ,C与Na反应生成D,则D为
,C与Na反应生成D,则D为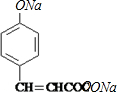 ,据此进行解答.
,据此进行解答.
解答 解:由信息①知,A分子含有酚羟基,两个取代基在苯环的对位;I催化氧化生成J,J能发生银镜反应,则I为CH3CH2OH、J为CH3CHO;A在浓硫酸作用下进行酯的水解反应生成B和I,根据B的分子式可知,B的不饱和度为$\frac{9×2+2-8}{2}$=6,苯环和1个羧基的不饱和度为:4+1=5,说明B的侧链中还含有1个碳碳双键,则B为 、A为
、A为 ;B与HCl发生加成反应生成E,则E为
;B与HCl发生加成反应生成E,则E为 ;E与氢氧化钠溶液加热反应生成F,则F为
;E与氢氧化钠溶液加热反应生成F,则F为 ,F在酸性条件下转化成G,则G为
,F在酸性条件下转化成G,则G为 ;两分子G之间发生酯化反应生成H;B与碳酸氢钠反应生成C,则C为
;两分子G之间发生酯化反应生成H;B与碳酸氢钠反应生成C,则C为 ,C与Na反应生成D,则D为
,C与Na反应生成D,则D为 ,
,
(1)根据分析可知,I为CH3CH2OH乙醇,名称为乙醇;J为乙醛.G发生分子间酯化反应生成H,酯化反应也是取代反应,
故答案为:乙醇;取代反应(或酯化反应);
(2)B为 ,B的官能团有碳碳双键、羟基、羧基,其中含氧官能团为羟基和羧基;E在氢氧化钠溶液中反应生成F,发生反应的类型为水解反应和中和反应,反应的化学方程式为:
,B的官能团有碳碳双键、羟基、羧基,其中含氧官能团为羟基和羧基;E在氢氧化钠溶液中反应生成F,发生反应的类型为水解反应和中和反应,反应的化学方程式为:
故答案为:羟基、羧基;
(3)已知:ROH+R1Cl$→_{△}^{催化剂}$ROR1+HCl,C与E以物质的量比1:1混合在催化剂、加热条件下反应,根据已知条件可知,C和E发生了取代反应,反应的化学方程式为: +
+ $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +HCl,
+HCl,
故答案为: +
+ $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +HCl.
+HCl.
点评 本题考查了有机推断,题目难度较大,熟练掌握常见有机物结构与性质为解答关键,题干信息为解答突破口,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及灵活应用基础知识的能力,是一道质量不错的练习.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:解答题
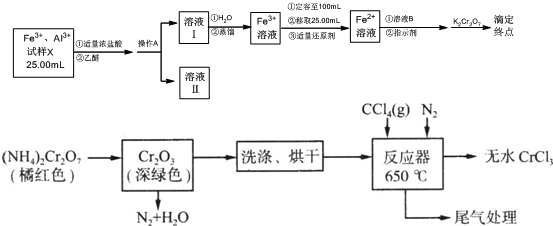
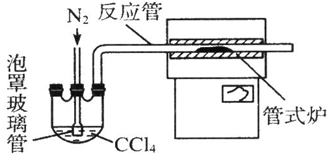
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
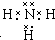 .在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是2NH3•H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2+6H2O.
.在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是2NH3•H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
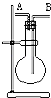 某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )
某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:①H2; ②Cl2;③SO2;④HCl;⑤NH3;⑥NO;⑦NO2.下列说法正确的是( )| A. | 烧瓶是干燥的,由B进气,可收集②③④⑥⑦ | |
| B. | 烧瓶是干燥的,由A进气,可收集①⑤ | |
| C. | 在烧瓶中充满水,由A进气,可收集①⑤⑦ | |
| D. | 在烧瓶中充满水,由B进气,可收集⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com