
| A. | △H3+2△H1+2△H2 | B. | △H3+2△H1+△H2 | C. | △H3+2△H1-△H2 | D. | △H3+2△H1-2△H2 |
分析 ①C(s)+O2(g)═CO2(g)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g)△H3
则③+2×①-②可得:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g),依据盖斯定律计算反应的热效应.
解答 解:①C(s)+O2(g)═CO2(g)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g)△H3
则③+2×①-②可得:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g),依据盖斯定律可知:TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H为△H3+2△H1-△H2;
故选:C.
点评 本题考查了反应热的计算,侧重考查利用盖斯定律计算反应的热效应,解题关键准确利用已知反应通过混合运算得到目标方程式,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
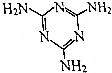 三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )
三聚氰胺的结构式如图所示,尿素[CO(NH2)2]在一定条件下发生分解反应可制得三聚氰胺和CO2等物质,下列说法不正确的是( )| A. | 三聚氰胺的分子式为C3H6N6 | |
| B. | 氰胺的结构简式为H2N-C≡N | |
| C. | 尿素分解制三聚氰胺时,除生成CO2外,还会生成NH3 | |
| D. | 三聚氰胺属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 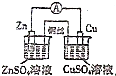 设计铜锌原电池 | B. |  制备氢氧化亚铁并观察其颜色 | ||
| C. |  定量测定H2O2的分解速率 | D. |  证明铁生锈与空气有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
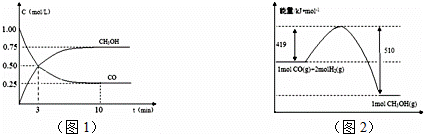
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2g | B. | 3g | C. | 3.5g | D. | 4.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂试剂或操作方法 | |
| A. | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| B. | FeSO4 | CuSO4 | 加入NaOH溶液,过滤 |
| C. | NaCl溶液 | I2 | 加酒精,萃取分液 |
| D. | KNO3溶液 | AgNO3 | 加入NaCl溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
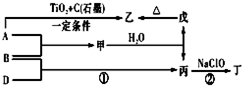 已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol 丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件巳略去).
已知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol 丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件巳略去). .写出丙的结构式
.写出丙的结构式 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com