
·ÖĪö £Ø1£©øĆ·“Ó¦ÖŠCuŌŖĖŲ»ÆŗĻ¼ŪÓÉ+1¼Ū±äĪŖ+2¼Ū”¢NŌŖĖŲ»ÆŗĻ¼ŪÓÉ+5¼Ū±äĪŖ+2¼Ū£¬øł¾Ż×ŖŅʵē×ÓŹŲŗć”¢µēŗÉŹŲŗć¼°Ō×ÓŹŲŗćÅäĘ½·½³ĢŹ½£»
£Ø2£©·“Ó¦ŗóµÄČÜŅŗÖŠČÜÖŹŗĶNaOH·¢Éśø“·Ö½ā·“Ӧɜ³ÉĻõĖįÄĘ£¬øł¾ŻÄĘŌ×ÓŹŲŗć¼ĘĖć·“Ó¦ČÜŅŗÖŠn£ØNO3-£©£¬ŌĄ“ČÜŅŗÖŠn£ØHNO3£©=n£ØNO3-£©£Ø·“Ó¦ŗóČÜŅŗÖŠ£©+n£ØNO£©£¬ŌŁ½įŗĻc=$\frac{n}{V}$¼ĘĖćŌĄ“ČÜŅŗÖŠĻõĖįÅØ¶Č£»
£Ø3£©øł¾Ż×ŖŅʵē×ÓŹŲŗć¼ĘĖćŌ»ģŗĻĪļÖŠCu2OµÄÖŹĮ森
½ā“š ½ā£ŗ£Ø1£©øĆ·“Ó¦ÖŠCuŌŖĖŲ»ÆŗĻ¼ŪÓÉ+1¼Ū±äĪŖ+2¼Ū”¢NŌŖĖŲ»ÆŗĻ¼ŪÓÉ+5¼Ū±äĪŖ+2¼Ū£¬×ŖŅʵē×ÓŹżĪŖ6£¬øł¾Ż×ŖŅʵē×ÓŹŲŗć”¢µēŗÉŹŲŗć¼°Ō×ÓŹŲŗćÅäĘ½·½³ĢŹ½ĪŖ3Cu2O+14H++2NO3-ØT6Cu2++2NO”ü+7H2O£¬
¹Ź“š°øĪŖ£ŗ3£»13£»2£»6£»2£»7£»
£Ø2£©·“Ó¦ŗóµÄČÜŅŗÖŠČÜÖŹŗĶNaOH·¢Éśø“·Ö½ā·“Ӧɜ³ÉĻõĖįÄĘ£¬øł¾ŻÄĘŌ×ÓŹŲŗćµĆn£ØNaOH£©=n£ØNO3-£©=6mol/L”Į0.2L=1.2mol£¬ŌĄ“ČÜŅŗÖŠn£ØHNO3£©=n£ØNO3-£©£Ø·“Ó¦ŗóČÜŅŗÖŠ£©+n£ØNO£©=1.2mol+$\frac{4.48L}{22.4L/mol}$=1.4mol£¬ĻõĖįµÄc=$\frac{n}{V}$=$\frac{1.4mol}{0.5L}$=2.8mol/L£¬¹Ź“š°øĪŖ£ŗ2.8mol/L£»
£Ø3£©ÉčCuµÄĪļÖŹµÄĮæĪŖxmol”¢Cu2OµÄĪļÖŹµÄĮæĪŖymol£¬øł¾Ż×ŖŅʵē×ÓŹŲŗć”¢ÖŹĮæĮŠ·½³Ģ×éµĆ
$\left\{\begin{array}{l}{64x+144y=27.2}\\{2x+2y=0.2mol”Į3}\end{array}\right.$
½āµĆ$\left\{\begin{array}{l}{x=0.2}\\{y=0.1}\end{array}\right.$£¬
Ōņm£ØCu2O£©=144g/mol”Į0.1mol=14.4g£¬
“š£ŗŌ»ģŗĻĪļÖŠCu2OµÄÖŹĮæŹĒ14.4g£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļµÄ¼ĘĖć”¢»Æѧ·½³ĢŹ½µÄÅäĘ½µČÖŖŹ¶µć£¬²ąÖŲæ¼²éѧɜ·ÖĪö¼ĘĖćÄÜĮ¦£¬Ō×ÓŹŲŗć”¢×ŖŅʵē×ÓŹŲŗćŹĒ½ā“šøĆĢāµÄ½ĻŗĆ·½·Ø£¬×¢Ņā£Ø2£©ĢāµÄĒÉĆī·ÖĪö£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĒāŃõ»ÆĪļ | Fe£ØOH£©3 | Al£ØOH£©3 | Mg£ØOH£©2 |
| æŖŹ¼³ĮµķpH | 2.7 | 3.7 | 9.6 |
| ĶźČ«³ĮµķpH | 3.7 | 4.7 | 11 |
| ĪĀ¶Č/”ę | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3µÄČܽā¶Č/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ź±¼ä£Øs£© | 0 | 1 | 2 | 3 | 4 | 5 |
| n£ØNO£©£Ømol£© | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĘČ”25gµØ·ÆČܽāŌŚ1LĖ®ÖŠ | |
| B£® | ½«16gµØ·ÆČÜÓŚĖ®£¬Č»ŗ󽫓ĖČÜŅŗĻ”ŹĶÖĮ1L | |
| C£® | ³ĘČ”25gµØ·ÆČÜÓŚĖ®£¬Č»ŗ󽫓ĖČÜŅŗĻ”ŹĶÖĮ1L | |
| D£® | ½«µØ·Æ¼ÓČČ³żČ„½į¾§Ė®ŗ󣬳ĘČ”16gČܽāŌŚ1LĖ®ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | äåŅŅĶéµÄĻūČ„·“Ó¦£ŗCH3CH2Br+NaOH$”ś_{”÷}^{H_{2}O}$CH2ØTCH2”ü+NaBr+H2O | |
| B£® | ±½·ÓÄĘČÜŅŗÖŠĶØČėCO2£ŗ2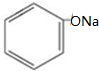 +CO2+H2O”ś2 +CO2+H2O”ś2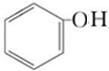 +Na2CO3 +Na2CO3 | |
| C£® | ŗĻ³É¾Ū±ūĻ©ĖÜĮĻ£ŗnCH2=CH-CH3$\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$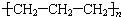 | |
| D£® | ŅŅČ©ÓėŠĀÖĘŅų°±ČÜŅŗ·“Ó¦£ŗCH3CHO+2Ag£ØNH3£©2OH$\stackrel{Ė®ČÜŅŗ¼ÓČČ}{”ś}$CH3COONH4+2Ag”ż+3NH3+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Č”“ś””¼Ó³É””Ė®½ā | B£® | ĻūČ„””¼Ó³É””Ė®½ā | C£® | Ė®½ā””ĻūČ„””¼Ó³É | D£® | ĻūČ„””Ė®½ā””Č”“ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
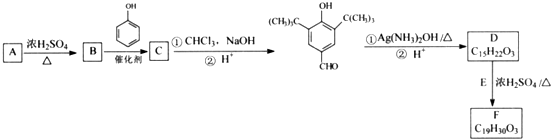
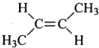
 £ØR“ś±ķĢž»ł£©
£ØR“ś±ķĢž»ł£©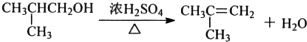 £»
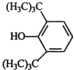
£» £»
£» £»
£»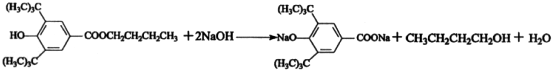 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com