
化学与人类社会可持续发展密切相关,能源、环境、工业生产以及日常生活等都离不开化学。
(1)大量使用化石燃料,最直接的危害是造成大气污染,如“温室效应”、“酸雨”等都与大量使用化石燃料有关。为了防治酸雨,降低煤燃烧时向大气排放的SO2,国际上最新采用“饱和亚硫酸钠溶液吸收法”,请写出有关反应的化学方程式_______________。
(2)燃煤过程中生成的SO 2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl222.4L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是 。
2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl222.4L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是 。
(3)三硅酸镁(Mg2Si3O8·nH2O)难溶于水,在医药上可做抗酸剂。它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激。三硅酸镁与盐酸反应的化学方程式为______________。将0.184 g三硅酸镁加到50 mL 0.1 mo1·L-1盐酸中,充分反应后,滤去沉淀,以甲基橙为指示剂,用 0.1 mo1·L-1NaOH溶液滴定剩余的盐酸,消耗NaOH溶液30 mL,则Mg2Si3O8·nH2O的n值为________________。(注:Mg2Si3O8的摩尔质量为260 g·mol-1)
科目:高中化学 来源:2017届广东省韶关市六校高三上10月联考化学试卷(解析版) 题型:实验题
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:
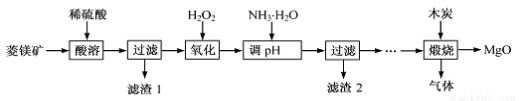
生成氢氧化物沉淀的pH:
Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 9.4 | 6.3 | 1.5 |
完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3 与稀硫酸反应的离子方程式为_______________________。
(2)加双氧水的目的______________________;相关的离子方程式_________________________;加氨水调节溶液的PH范围为______________。
(3)滤渣2 的成分是_____________(填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体可以是________________(填化学式)。
②B中盛放的溶液可以是________________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源:贵州省铜仁市2016-2017学年高一上期中化学试卷(解析版) 题型:实验题
铜仁一中高一年级某化学兴趣小组欲除去粗盐中的可溶性杂质CaCl2、MgCl2、 Na2SO4,他们先将粗盐溶于水,然后依次加入过量的溶液、NaOH溶液、
Na2SO4,他们先将粗盐溶于水,然后依次加入过量的溶液、NaOH溶液、 溶液,过滤后加过量的,最后经过操作,就得到了纯净的NaCl固体。
溶液,过滤后加过量的,最后经过操作,就得到了纯净的NaCl固体。
查看答案和解析>>
科目:高中化学 来源:贵州省铜仁市2016-2017学年高一上期中化学试卷(解析版) 题型:选择题
下列电解质溶于水时的电离方程式中,书写正确的是
A.H2SO3 2H++SO32-
2H++SO32-
B.NaHSO4=Na++H++SO42-
C.NaHCO3=Na++H++CO32-
D.K2SO4=K2++SO42-
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三10月月考化学试卷(解析版) 题型:选择题
蛇纹石由MgO、Al2O3,、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是
A.沉淀X的成分是SiO2
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3
C.在溶液Y中加入过量的NaOH溶液,过滤得到沉淀的主要成分是Fe(OH)3和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三10月月考化学试卷(解析版) 题型:选择题
下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上10月模块测试化学试卷(解析版) 题型:选择题
用离子方程式解释以下指定反应,书写正确的是( )
A.亚硫酸钠溶液显碱性:SO32-+2H2O=H2SO3+2OH-
B.(NH4)2FeSO4溶液与过量NaOH溶液混合制取氢氧化亚铁:Fe2++2OH-=Fe(OH)2
C.NaAlO 2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-
2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-
D.铁红溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三上统一考试化学试卷(解析版) 题型:填空题
氢能是理想的清洁能源,资源丰富。以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下:
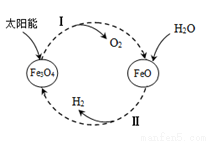
(1)过程Ⅰ:2Fe3O4(s)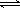 6FeO(s)+O2(g) ΔH=+313.18 kJ/mol
6FeO(s)+O2(g) ΔH=+313.18 kJ/mol
① 将O2分离出去,目的是提高Fe3O4的__________________。
② 平衡常数K随温度变化的关系是 。
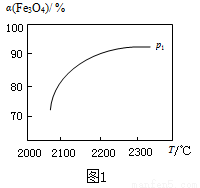
③ 在压强p1下,Fe3O4的平衡转化率随温度变化的α(Fe3O4)~T曲线如图1所示。若将压强由p1增大到p2,在图1中画出p2的α(Fe3O4)~T曲线示意图。
(2)过程Ⅱ的化学方程式是 。
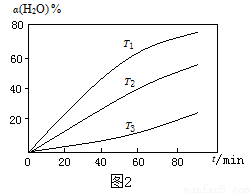
(3)过程Ⅱ,其他条件不变时,在不同温度下,H2O的转化率随时间的变化α(H2O)~t 曲线如图2所示。比较温度T1、T2、T3的大小关系是 ,判断依据是  。
。
(4)科研人员研制出透氧膜(OTM),它允许电子、O2-同时透过,可实现水连续分解制H2。工作时,CO、H2O分别在透氧膜的两侧反应。工作原理示意图如下:
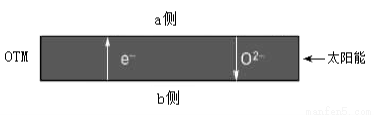
H2O在___________侧反应(填“a”或 “b”),在该侧H2O释放出H2的反应式是 。
“b”),在该侧H2O释放出H2的反应式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com