
| 实验编号 | 温度(℃) | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响;(Ⅱ)实验①和③探究温度对反应速率的影响;(Ⅲ)实验①和④探究大理石规格(粗、细)对反应速率的影响. |
| ② | ||||
| ③ | ||||
| ④ |
分析 根据实验目的“(Ⅰ)实验①和②探究浓度对反应速率的影响、(Ⅱ)实验①和③探究温度对反应速率的影响”及变量唯一性判断实验②③的反应条件;实验①和④探究应该探究大理石规格对反应速率的影响,据此解答④的反应条件.
解答 解:实验①和②探究浓度对反应速率的影响,则反应温度、大理石规格必须相同,只有硝酸的浓度不同;实验①③探究温度对反应速率的影响,则只有温度不同,其它条件完全相同;实验①④应该是探究大理石规格对反应速率的影响,则两个实验中应该只有大理石规格不同,据此完成表格为:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol•L-1 | 实验目的 |
| ① | 大理石规格(粗、细) | |||
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol•L-1 | 实验目的 |
| ① | 大理石规格(粗、细) | |||
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
点评 本题考查了探究影响化学法反应速率的因素,题目难度中等,明确对照实验设计方法为解答关键,注意掌握影响化学反应速率的因素,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 同一周期元素的原子,半径越小越容易失去电子 | |
| B. | 在同一周期中,ⅠA族单质的活泼性比ⅡA族的弱 | |
| C. | 所有主族元素的最高化合价数与它的族序数数值相等 | |
| D. | 同主族元素的气态氢化物,相对分子质量越大,沸点不一定越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
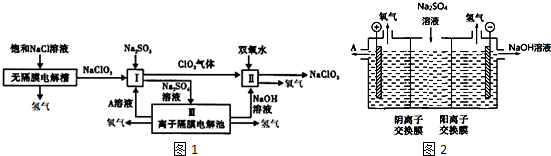
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKap | 37.4 | 19.3 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该元素的原子序数是72 | B. | 该元素的原子序数是185 | ||
| C. | 该原子相对原子质量是185 | D. | 该元素是一种新元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 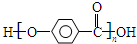 的结构中含有酯基 的结构中含有酯基 | |
| B. | 甲基的电子式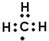 | |
| C. | 顺-2-丁烯和反-2-丁烯的加氢产物不同 | |
| D. | 用重结晶的方法提纯苯甲酸时应趁热过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com