
【题目】Ⅰ、下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法,用序号填空)。①溶解 ②裂解 ③分馏 ④裂化 ⑤干馏 ⑥蒸馏 ⑦过滤 ⑧电解 ⑨萃取
(1)将海水淡化 。
(2)从海水得到的无水MgC12中提取金属镁 。
Ⅱ、下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
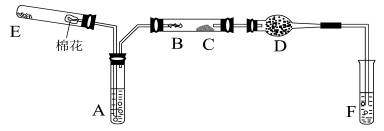
图中:A为无水乙醇(沸点为78℃),
B为绕成螺旋状的细铜丝或银丝,
C为无水CuSO粉末,
D为碱石灰,
F为新制的氢氧化铜悬浊液。
已知: 含—CHO的物质在加热条件下与新制的Cu(OH)2悬浊液反应生成砖红色沉淀.
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是_____________。
D处使用碱石灰的作是 。
(3) E处是一种纯净物,其反应方程式为 。
(4)写出乙醇发生催化氧化的化学方程式 。
【答案】I ⑥(2分),⑧ (2分) II (1)A、B、E、F (2分) (2)水浴加热, 防止F中的水进入C处(2分)(3)2KMnO4 ![]() K2MnO4 + MnO2 + O2 (2分) (4)2CH3CH2OH + O2
K2MnO4 + MnO2 + O2 (2分) (4)2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O(2分)
2CH3CHO + 2H2O(2分)
【解析】
试题分析:I:(1)从海水中获取淡水,可用蒸馏的方法分离,加热时水蒸发,冷却后可得到纯净水,故答案为:⑥;(2)Mg为活泼金属,工业用电解MgCl2的方法制得单质Mg,故答案为:⑧.Ⅱ、:(1)固体加热制氧气需要加热,乙醇变为蒸汽需加热,乙醇的催化氧化要加热,醛和与新制的Cu(OH)2悬浊液反应也要加热,故答案为: A、B、E、F;(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是水浴加热;碱石灰具有吸水作用,D处使用碱石灰可以防止F中的水蒸气进入C中与无水CuSO4作用,否则会影响产物水的检验,故答案为:水浴加热;防止F中的水蒸气进入C中与无水CuSO4作用,影响产物水的检验;(3)固体纯净物加热制氧气的只能是加热高锰酸钾制氧气,反应为:2KMnO4
![]() K2MnO4+MnO2+O2↑,答案为:2KMnO4
K2MnO4+MnO2+O2↑,答案为:2KMnO4![]() K2MnO4+MnO2+O2↑;(4)乙醇在通过催化剂时,可以被氧化为乙醛,反应的方程式为:2CH3CH2OH+O2
K2MnO4+MnO2+O2↑;(4)乙醇在通过催化剂时,可以被氧化为乙醛,反应的方程式为:2CH3CH2OH+O2![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。


科目:高中化学 来源: 题型:
【题目】某媒体以《中国酱油遭遇欧盟高门槛》为题,报道了我国广东某地生产的酱油很可能在欧洲市场被判死刑,从而失去几百万美元的份额一事,其原因是酱油中的氯丙醇严重超标.三氯丙醇(分子中只含一个羟基)的同分异构体有(—OH和—Cl不在同一个C原子上)( )
A. 3种 B. 4种 C. 5种 D. 6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 ,氧化性最弱的简单阳离子是 。
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是 ;
制铝时,电解Al2O3而不电解AlCl3的原因是 。
(4)晶体硅(熔点1410 ℃)是良好的半导体材料。由粗硅制纯硅过程如下:
![]()
写出SiCl4的电子式: ;在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式:
(5)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是
a.NH3 b.HI c.SO2 d.CO2
(6)KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:
(7)工业上,通过如下转化可制得KClO3晶体:![]()
完成Ⅰ中反应的总化学方程式:
![]()
Ⅱ该反应过程能析出KClO3晶体而无其他晶体析出的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一套电化学装置,如下图所示,E 为沾有 Na2SO4溶液的滤纸,并加入几滴酚酞。A、B分别为Pt片,压在滤纸两端,R、S为电源的电极。M、N是用多微孔的 Ni 制成的电极材料,它在碱性溶液中可以视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的 KMnO4溶液,断开K,接通外电源一段时间后,C、D中有气体产生。

(1)S为________(填“正”或“负”)极。
(2)A极附近溶液的现象是______________, B 极附近发生的电极反应式为___________。
(3)滤纸上的紫色点向______(填“A”或“B”)方移动。
(4)当 C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,D中的电极为________ (填“正”或“负”)极,电极反应式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有a mol/L 的NaX和b mol/L的NaY两种盐溶液。下列说法正确的是
A.若a=b且c(X-)= c(Y-)+ c(HY),则HX为强酸
B.若a=b且pH(NaX)>pH(NaY),则c(X-)+ c(OH-)> c(Y-)+ c(OH-)
C.若a>b且c(X-)= c(Y-),则酸性HX>HY
D.若两溶液等体积混合,则c(Na+)=(a+b) mol/L(忽略混合过程中的体积变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生反应后固体质量一定减少的是
A.FeCO3在空气中灼烧 B.铝条插入冷的浓硫酸中
C.Na2O2敞放在空气中 D.向Mg(OH)2悬浊液中加入FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列说法中不正确的是
A.蛋白质、棉花、PVC、淀粉都是混合物
B.废弃的玻璃、金属、纸制品是可回收利用的资源
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制下列溶液时常需加入少量括号内的物质,其中不是为了抑制离子水解的是
A.FeSO4(Fe) B.SnCl2(HCl) C.FeCl3(HCl) D.NaAlO2(NaOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为35℃,从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法、乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是__________;
(2)操作Ⅰ需要的玻璃仪器主要有:烧杯、玻璃棒、__________,操作Ⅱ的名称是__________;操作Ⅲ的名称是__________;
(3)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定青蒿素分子式的装置。
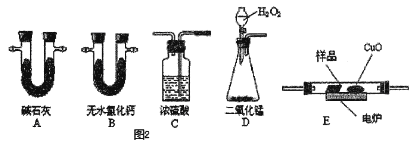
①按上述所给的测试信息。装置的连接顺序应是__________(每个装置限用一次)。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是__________;
③青蒿素样品的质量为28.2 g。用合理改进后的装置进行试验,称得A管增重66 g,B管增重19.8 g,则测得青蒿素的最简式是__________。
④要确定该有机物的分子式,还必须知道的数据是__________。
(4)某学生对青蒿素的性质进行探究.将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,与青蒿素化学性质相似的物质是__________(填字母代号)
A.乙醇 B.乙酸 C.葡萄糖 D.乙酸乙酯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com