
| 选项 | 实验操作 | 现象或结论 |
| A | 将铁屑、溴水、苯混合加热 | 制取溴苯 |
| B | 先加入浓硫酸,再加入苯,最后滴入浓硝酸 | 制取硝基苯 |
| C | 向C6H5ONa溶液巾通入CO2气体 | 溶液出现浑浊,证明酸性:C6H5OH<H2CO3 |
| D | 乙醇和浓硫酸混合加热,将产生的气体通人酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色,证明乙醇发生消去反应生成乙烯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯不与溴水反应,应该用液溴;
B.苯易挥发,应该冷却后最后加入苯;
C.根据强酸制取弱酸原理分析;
D.乙醇易挥发,挥发出的乙醇也能够使酸性高锰酸钾溶液褪色.
解答 解:A.苯与溴水不反应,应该将铁屑、液溴、苯混合加热无法制取溴苯,故A错误;
B.实验室制硝基苯时,先将浓HNO3注入容器中,然后再慢慢注入浓H2SO4,并及时搅拌,浓硝酸和浓硫酸混合后,在50-60℃的水浴中冷却后再滴入苯,故B错误;
C.向C6H5ONa溶液中通入CO2气体,溶液出现浑浊,说明有苯酚生成,可证明酸性:C6H5OH<H2CO3,故C正确;
D.乙醇和浓硫酸混合加热,乙醇易挥发,则制取的乙烯中混有乙醇,干扰了检验结果,无法达到实验目的,故D错误;
故选C.
点评 本题考查化学实验方案的评价,题目难度不大,涉及溴苯、硝基苯制取、酸性强弱比较、乙烯检验等知识,明确常见有机物制备原理及检验方法为解答关键,试题培养了学生的化学实验能力.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:选择题
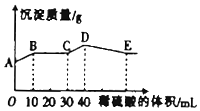 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合液中滴加1mol•L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是( )| A. | AB段发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ | |
| B. | E点对应横坐标稀硫酸的体积为70mL | |
| C. | D点表示的沉淀的化学式为Al(OH)3、BaSO4 | |
| D. | E点沉淀比A点沉淀质量大2.33g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaO2的水解产物是Ba(OH)2和H2O2 | B. | PCl3水解的产物是HClO和PH3 | ||
| C. | CaC2水解的产物是Ca(OH)2和C2H2 | D. | Al2S3水解的产物是Al(OH)3和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向蒸馏水中滴加浓硫酸的过程中,Kw保持不变 | |
| B. | 酸与碱溶液恰好完全反应时所得溶液一定呈中性 | |
| C. | 向醋酸钠溶液中加入少量冰醋酸,水的电离度减小 | |
| D. | 广泛pH试纸能够测出溶液的精确pH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
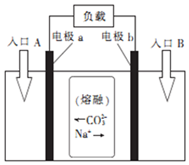 “直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能.用熔融Na2CO3作电解质的直接煤燃料电池的工作原理如图.下列有关说法正确的是( )
“直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能.用熔融Na2CO3作电解质的直接煤燃料电池的工作原理如图.下列有关说法正确的是( )| A. | 该电池的总反应为C+O2═CO2 | |
| B. | 煤直接燃烧发电比直接煤燃料电池发电的能量利用率高 | |
| C. | 进入反应室的煤块粉碎成粉末状对反应速率和限度均无影响 | |
| D. | 电子由电极b沿导线流向电极a,入口A加入的物质为煤粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 将过量氨水加入AlCl3溶液中:Al3++4OH-═AlO2-+2H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+5I-+6H+═3I2+3H2O | |
| D. | 向NaHCO3溶液中加入等物质的量的Ca(OH)2:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | O=O | H-O |
| 键能(KJ/mol) | 436 | 496 | 463 |
| A. | 242KJ | B. | 442 KJ | C. | 484 KJ | D. | 448KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com