
| A. | 单位时间内生成n mo1 O2的同时生成n mol NO2 | |
| B. | 单位时间内生成n mol O2的同时生成2n molNO | |
| C. | 混合气体的颜色不再改变 | |
| D. | 混合气体的平均密度不再改变的状态 |
分析 可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质物质的量不变、物质的量浓度不变、百分含量不变以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.单位时间内生成n mo1 O2的同时生成2n mol NO2时该反应达到平衡状态,所以当单位时间内生成n mo1 O2的同时生成n mol NO2时该反应没有达到平衡状态,平衡向逆反应方向移动,故A错误;
B.无论反应是否达到平衡状态,都存在单位时间内生成n mol O2的同时生成2n molNO,所以不能据此判断平衡状态,故B错误;
C.该反应中只有二氧化氮是有色气体,当混合气体的颜色不变时,说明二氧化氮含量不变,正逆反应速率相等,该反应达到平衡状态,故C正确;
D.反应前后气体质量不变、容器体积不变,所以密度始终不变,不能据此判断平衡状态,故D错误;
故选C.
点评 本题考查化学平衡状态判断,为高频考点,只有反应前后改变的物理量不变时该反应才能达到平衡状态,为易错题.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 该溶液物质的量浓度为10moL/L | |
| B. | 所得的溶液的体积为22.5L | |
| C. | 该溶液中溶质的质量分数因溶液的密度未知而无法求得 | |
| D. | 根据题干数据,该溶液物质的量浓度无法求得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
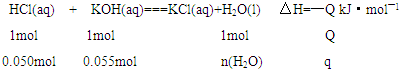
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.3mol•L-1的Na2SO4溶液 | B. | 4L 0.5mol•L-1的NaCl溶液 | ||
| C. | 2L 0.3mol•L-1的NaOH的溶液 | D. | 1L 0.15mol•L-1的Na3PO4的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
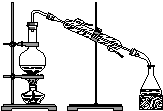 | 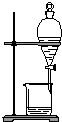 |  | 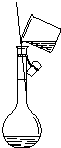 |
| A用海水制蒸馏水 | B将碘水中的碘单质与水直接分离 | C除去Fe(OH)3胶体中的FeCl3 | D稀释浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于15.0mL | B. | 等于15.0mL | C. | 小于15.0mL | D. | 等于10.0mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4与稀硝酸反应:Fe3O4+8 H+═2Fe3+十Fe2++4H2O | |
| B. | 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++So4 2-═BaSO4↓ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 含0.4mol FeBr2溶液与0.4mol Cl2恰好反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2为0.4mol/L、O2为0.2mol/L | B. | SO3为0.4mol/L | ||
| C. | SO2、SO3均为0.15mol/L | D. | SO3为0.25mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用如图所示装置,制备并收集少量NO2气体 | |
| B. |  用如图所示装置,除去CO2中的HCl | |
| C. |  用图所示装置,制备Fe(OH)2并能较长时间观察其颜色 | |
| D. |  用图所示装置,所示装置制取并收集干燥纯净的NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com