
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 7.8gNa2O2中含有阴离子数目为0.2NA | |
| C. | 71g氯气溶于水配成溶液,所得溶液中含Cl-数目为1 NA | |
| D. | 4℃,18g水所含分子数目为NA |
分析 A.计算物质的量n=$\frac{m}{M}$,金属镁核外12个电子;
B.求出Na2O2的物质的量,然后根据1molNa2O2含2molNa+和1molO22-来分析;
C.计算物质的量n=$\frac{m}{M}$,氯气和水反应是可逆反应;
D.4℃,18g水物质的量=$\frac{18g}{18g/mol}$=1mol,含分子数1mol.
解答 解:A、2.4g镁的物质的量是0.1mol,含有1.2mol电子,所含电子数目为1.2NA,故A错误;
B.7.8gNa2O2的物质的量为0.1mol,而1molNa2O2含2molNa+和1molO22-,故0.1molNa2O2含0.1molO22-,故B错误;
C.71g氯气物质的量=$\frac{71g}{71g/mol}$=1mol,氯气和水反应生成盐酸和次氯酸,反应为可逆反应,溶液中氯离子物质的量小于1mol,故C错误;
D.18g水的物质的量为1mol,含有分子数目为NA,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:选择题
| A. | 加热煮沸的主要目的是除去溶液中溶解的氯气 | |
| B. | 稀释过程中用到的玻璃仪器主要有烧杯、玻璃棒、胶头滴管 | |
| C. | 滴定过程中可用KSCN溶液作指示剂 | |
| D. | 铁矿石中铁的质量分数为70% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制乙烯时,温度计水银球应插入混合液中,而石油分馏时则不能插入混合液中 | |
| B. | 实验室用溴和苯在铁粉存在下反应,得到的溴苯显褐色,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 | |
| C. | 检验2-溴丙烷中的溴原子:加入NaOH水溶液共热,冷却后,用稀硝酸酸化后再滴入AgNO3溶液,观察有淡黄色沉淀生成 | |
| D. | 制取硝基苯时,应取1.5 mL浓HNO3,加入浓H2SO4 2mL,冷却至50℃以下,再滴入苯约1mL,然后放在水浴中加热,温度计应放在混合液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
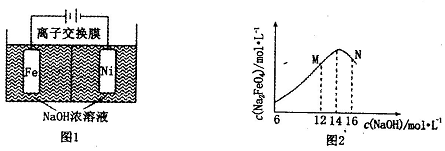
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅胶作袋装食品的干燥剂 | |
| B. | 氯气作自来水杀菌消毒剂 | |
| C. | 用铂丝蘸取碳酸钠溶液在酒精灯外焰上灼烧 | |
| D. | 用蒸馏的方法除去自来水中的Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶 | |
| B. | 蔗糖、酒精在水溶液或熔融状态下均不导电,所以它们均是非电解质 | |
| C. | 硅的性质稳定,所以在自然界中可以以游离态存在 | |
| D. | 电泳现象可证明胶体带电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com