
下表是周期表中一部分,根据A~M在周期表中的位置,按要求回答下列问题:(用相关的元素符号或分子式表示)

(1)表中元素,只有负价而无正价的元素是________,氧化性最强的单质是________,化学性质最不活泼的元素是________,金属性最强的单质与水反应的化学方程式是________.
(2)最高价氧化物对应的水化物酸性最强的是,呈两性的是________.
(3)元素F形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是________,该化合物的颜色为________色.
(4)元素M的单质和石灰乳作用可制成有漂白和消毒作用的漂白粉,用化学方程式表示漂白粉在潮湿空气中起漂白作用的原理________.
|
答案:(1)F F2 Ne 2Na+2H2O (2)HClO4 Al(OH)3 (3)2Na2O2+2CO2 (4)Ca(ClO)2+CO2+H2O 解析:根据元素在周期表中的位置,可知A为H,B为C,C为N,D为F,E为Ne,F为Na,G为Mg,H为Al,I为Si,J为P,K为S,M为Cl.在这12种元素中,F是非金属性最强的元素,只有负价而无正价,其单质氧化性最强;Ne是稀有气体,化学性质最不活泼;金属性最强的是Na;最高价氧化物对应水化物酸性最强的是HClO4,呈两性的Al(OH)3,Na2O2与CO2反应能生成O2,所以Na2O2可作呼吸面具中的供氧剂;漂白粉中的Ca(ClO)2与空气中的CO2和H2O反应生成具有漂白作用的HClO. |


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
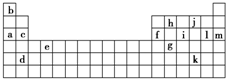 下表是周期表的一部分,表中所列的字母分别代表某一化学元素.
下表是周期表的一部分,表中所列的字母分别代表某一化学元素.| 锂 | X | Y | |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | 9 550 | 11 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族周期 | ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | J | K |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 周期 | ||||||||
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
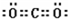
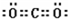
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com