
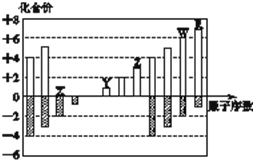
 如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图所示是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A、原子半径:Z>Y>X |
| B、气态氢化物的稳定性:R>W |
| C、WX3和水反应形成的化合物是离子化合物 |
| D、Y和Z两者最高价氧化物对应的水化物不能相互反应 |


科目:高中化学 来源: 题型:
| A、加入氨水,产生白色沉淀,证明原溶液中存在Al3+ |
| B、加入AgNO3溶液,产生白色沉淀,证明原溶液中存在Cl- |
| C、加入盐酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中存在SO42- |
| D、加入NaOH溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中存在NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(H2)=0.03mol?L-1?min-1 |
| B、v(N2)=0.02mol?L-1?min-1 |
| C、v(NH3)=0.17mol?L-1?min-1 |
| D、v(NH3)=0.01mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中Se是氧化产物,I2是还原产物 |
| B、SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是I2>SeO2>H2SO4(浓) |
| C、常温常压下,Se是固体,其最高价氧化物对应的水化物是H2SeO4 |
| D、反应①中每有0.6mol I2生成,转移电子数目为2.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 钾 | 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 774 | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com