
a mol FeS与b mol Fe3O4投入到V L c mol·L-1的硝酸溶液中恰好完全反应,假设只产生
NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
A.(a+3b) mol B.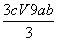 mol
mol
C.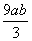 mol D.(cV-3a-9b) mol
mol D.(cV-3a-9b) mol
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
A.常温下,23g NO2含有NA个氧原子
B.1L 0.1mol·L-1的氨水含有0.1NA个OH-
C.常温常压下,22.4LCCl4含有个NA个CCl4分子
D.1molFe2+ 与足量的H2O2溶液反应,转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各装置图的叙述中,不正确的是 ( )
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
硝基苯是重要的精细化工原料,是医药和染料的中间体,还可做有机溶剂。制备硝基苯的组装如下图反应装置,过程如下:

步骤:取100 mL烧杯,用20 mL浓硫酸与浓硝酸18 mL配制混和酸,加入恒压漏斗中。把18 mL苯加入三颈烧瓶中。
②向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。
③在50-60℃下发生反应,直至反应结束。
④将反应后的液体依次用蒸馏水和10%Na2CO3溶液洗涤,最后再用蒸馏水洗涤得到粗产品。
请回答下列问题:
(1)配置混酸应先在烧杯中先加入 。
(2)恒压滴液漏斗的优点是 。
(3)实验装置中长玻璃管可用 代替(填仪器名称)。
(4)反应结束后产品在液体的 层(填“上”或者“下”),分离混酸和产品的操作方法为 。
(5)为了得到更纯净的硝基苯,还须先向液体中加入 除去水,然后蒸馏。
(6)写出制备硝基苯的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.小苏打溶液呈碱性的原因:HCO3-+H2O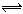 H3O++CO32-
H3O++CO32-
C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl-
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:
NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或对实验事实的描述正确的是( )
A.欲将蛋白质从水中析出而又不改变它的性质,应加入CuSO4溶液
B.乙醇可以被氧化为乙酸,二者都能发 生酯化反应
生酯化反应
C.淀粉溶液中加入一定量稀硫酸,共热一段时间后,向溶液中加入新制氢氧化铜悬浊液并加热煮沸,未见红色固体产生,证明淀粉没有发生水解
D.可用NaOH溶液除去混在乙酸乙酯中的乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列叙述正确的是( )
A.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
B.2 L0.5 mol • L-1硫酸钾溶液中阴离子所带电荷数为NA
C.1 mol Na2O2固体中含离子总数为4NA
D. 5NH4NO3 2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 gN2时,转移的电子数目为3.75NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com