
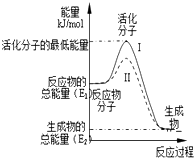
 ·“Ó¦aA£Øg£©+bB£Øg£©$\stackrel{“߻ƼĮ}{?}$cC£Øg£©£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ£®øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£ŗ±Č½ĻµŚ¢ņ½×¶Ī·“Ó¦ĪĀ¶Č£ØT2£©ŗĶµŚ¢ó½×¶Ī·“Ó¦ĪĀ¶Č£ØT3£©µÄøßµĶ£ŗT2__T3£Ø””””£©
·“Ó¦aA£Øg£©+bB£Øg£©$\stackrel{“߻ƼĮ}{?}$cC£Øg£©£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ£®øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚ¢ń”¢¢ņ”¢¢ó½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£ŗ±Č½ĻµŚ¢ņ½×¶Ī·“Ó¦ĪĀ¶Č£ØT2£©ŗĶµŚ¢ó½×¶Ī·“Ó¦ĪĀ¶Č£ØT3£©µÄøßµĶ£ŗT2__T3£Ø””””£©| A£® | £¾ | B£® | = | ||
| C£® | £¼ | D£® | Ģõ¼ž²»×ć£¬ĪŽ·ØÅŠ¶Ļ |
·ÖĪö “Ė·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬½µµĶĪĀ¶Č£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬Ę½ŗāµÄŅʶÆÖ»ÄܼõČõøı䣬²»ÄܵÖĻūøı䣬ÓÉ“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗµŚ¢ó½×¶ĪµÄæŖŹ¼ÓėµŚ¢ņ½×¶ĪµÄĘ½ŗāø÷ĪļÖŹµÄĮæ¾łĻąµČ£¬øł¾ŻA”¢BµÄĮæ¼õÉŁ£¬CµÄĮæŌö¼ÓæÉÅŠ¶ĻĘ½ŗāŹĒÕżĻņŅĘ¶ÆµÄ£¬øł¾ŻĘ½ŗāæŖŹ¼Ź±ÅضČČ·¶Ø“ĖĘ½ŗāŅĘ¶Æ²»æÉÄÜŹĒÓÉÅØ¶ČµÄ±ä»ÆŅżĘšµÄ£¬ĮķĶāĢāÄæĖłøųĢõ¼žČŻĘ÷µÄĢå»ż²»±ä£¬ŌņøıäŃ¹ĒæŅ²²»æÉÄÜ£¬Ņņ“ĖŅ»¶ØĪŖĪĀ¶ČµÄÓ°Ļģ£¬“Ė·“Ó¦ÕżĻņĪŖ·ÅČČ·“Ó¦£¬æÉŅŌĶĘ²āĪŖ½µµĶĪĀ¶Č£¬Ņņ“Ė“ļµ½Ę½ŗāŗóĪĀ¶ČŅ»¶Ø±ČµŚ¢ņ½×¶ĪĘ½ŗāŹ±µÄĪĀ¶ČµĶ£¬¹ŹŃ”£ŗA£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦ĖŁĀŹÓė»ÆŃ§Ę½ŗāĶ¼Ļ󔢻ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲµČ£¬ÄѶČÖŠµČ£¬Ń§ÉśÓ¦×¢Ņā»ÆŃ§Ę½ŗāŅʶÆŌĄķµÄÓ¦ÓĆ£®


 æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø
æŖŠÄæģĄÖ¼ŁĘŚ×÷ŅµŹī¼Ł×÷ŅµĪ÷°²³ö°ęÉēĻµĮŠ“š°ø ĆūĢāѵĮ·ĻµĮŠ“š°ø
ĆūĢāѵĮ·ĻµĮŠ“š°ø ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
ĘŚÄ©¼Æ½įŗÅĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £Ø1£©ŅŃÖŖ£ŗ
£Ø1£©ŅŃÖŖ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | F-µÄ½į¹¹Ź¾ŅāĶ¼£ŗ | B£® | CH4·Ö×ӵıȥżÄ£ŠĶ£ŗ | ||
| C£® | CCl4µÄµē×ÓŹ½£ŗ | D£® | ¼×ĶéµÄ½į¹¹¼ņŹ½£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
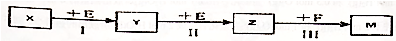
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ö±½ÓĮ¬½ÓX”¢Y£¬ŌņøĆ×°ÖĆæɽ«µēÄÜ×Ŗ±äĪŖ»ÆѧÄÜ | |
| B£® | Ö±½ÓĮ¬½ÓX”¢Y£¬Éś³É2.24LH2Ź±Ņ»¶Ø×ŖŅĘ0.2mole- | |
| C£® | ½«X”¢YÓėÖ±Į÷µēŌ“ĻąĮ¬£¬Ņ»¶ĪŹ±¼äŗó£¬Znʬ֏ĮæŅ»¶Ø¼õÉŁ | |
| D£® | ½«X”¢YÓėÖ±Į÷µēŌ“ĻąĮ¬£¬ŌņøĆ×°ÖĆæÉÄÜ·¢Éś·“Ó¦£ŗCu+H2SO4$\frac{\underline{\;Ķصē\;}}{\;}$CuSO4+H2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1mol/L | B£® | 10mol/L | C£® | 0.01mol/L | D£® | 0.1mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| W | µ„ÖŹŹĒµ»ĘÉ«¹ĢĢå |
| X | ŌŚµŲæĒÖŠµÄŗ¬Įæ¾ÓµŚ¶žĪ» |
| Y | Ō×Ó×īĶā²ćµē×ÓŹżŹĒµē×Ó×ÜŹżµÄ$\frac{2}{3}$ |
| Z | µŚČżÖÜĘŚŌ×Ó°ė¾¶×īŠ”µÄ½šŹō |
| A£® | ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗX£¾W | |
| B£® | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ£ŗY£¾X | |
| C£® | Ąė×Ó°ė¾¶£ŗZ£¾W | |
| D£® | XŌŚ×ŌČ»½ēÖŠŅŌÓĪĄėĢ¬ŗĶ»ÆŗĻĢ¬ŠĪŹ½“ęŌŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©ÄÜŹ¹äåĖ®ĶŹÉ« | |
| B£® | ŅŅĻ©ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« | |
| C£® | ½«±½¼ÓČėäåĖ®ÖŠ£¬Ņņ±½ÄÜÓėäåĖ®·¢Éś¼Ó³É·“Ó¦¶ųŹ¹äåĖ®ĶŹÉ« | |
| D£® | 50”«60”ꏱ£¬ŌŚÅØĮņĖį“ęŌŚĻĀ£¬±½ÄÜÓėÅØĻõĖį·“Ӧɜ³ÉĻõ»ł±½ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com