

分析 A、B、C、D、E5种短周期元素,它们的核电荷数依次增大,且都小于20,B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,最外层电子排布为ns2np4,则B为O元素、D为S元素;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,E的原子序数大于硫,且5种元素中只有C、E是金属元素,则A为H元素、E为K元素;C原子最外层上电子数等于D原子最外层上电子数的一半,其最外层电子数为6×$\frac{1}{2}$=3,故C为Al,以此解答该题.
解答 解:A、B、C、D、E5种短周期元素,它们的核电荷数依次增大,且都小于20,B和D属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,最外层电子排布为ns2np4,则B为O元素、D为S元素;A和E属同一族,它们原子的最外层电子排布为ns1,处于IA族,E的原子序数大于硫,且5种元素中只有C、E是金属元素,则A为H元素、E为K元素;C原子最外层上电子数等于D原子最外层上电子数的一半,其最外层电子数为6×$\frac{1}{2}$=3,故C为Al,
(1)由上述分析可知,A为H元素,B为O元素,C为Al元素,D为S元素,E为K元素,
故答案为:H;O;Al;S;K;
(2)由这五种元素组成的一种化合物的化学式为KAl(SO4)2.12H2O,该物质的一种主要用途:用作净水剂,
故答案为:KAl(SO4)2.12H2O;用作净水剂;
(3)C为Al元素,原子核外有13个电子,基态原子的电子排布式为1s22s22p63s23p1,
故答案为:1s22s22p63s23p1;
(4)D为S元素,基态原子最外层电子排布式为3s23p4,其轨道排布式为 ,故答案为:
,故答案为: ;
;
(5)同主族自上而下电负性降低,故电负性O>S,金属性越强,第一电离能越小,故第一电离能Al>K,
故答案为:O>S;Al>K.
点评 本题考查结构位置关系、元素周期表,为高考常见题型,元素的推断是解答的关键,侧重对核外电子排布的考查,旨在考查学生对基础知识的掌握,难度不大.


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:解答题
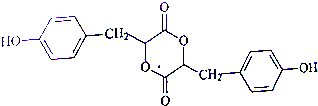
 .
.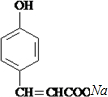 +
+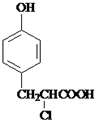 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +HCl.
+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ③⑤⑥ | C. | ②④⑤ | D. | 全部错误 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol | B. | 0.4 mol | C. | 0.8 mol | D. | 0.9 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
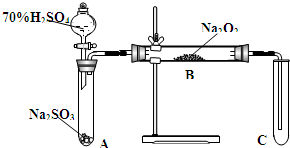 类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.
类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.查看答案和解析>>
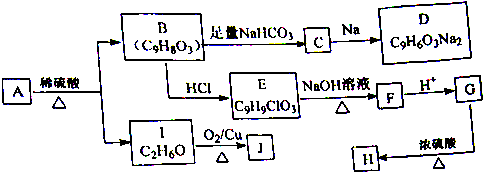
科目:高中化学 来源: 题型:推断题
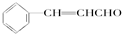 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的: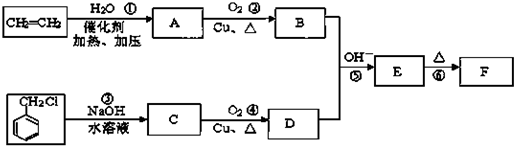
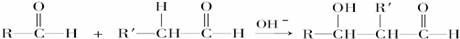
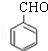 ;
;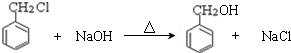 ,判断有关反应的类型:⑥消去反应;
,判断有关反应的类型:⑥消去反应;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中C失去电子,被还原 | |
| B. | 该反应中氢气得到电子,被还原 | |
| C. | 该反应中,每转移2mole-则生成1mol氢气. | |
| D. | 该反应属于复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com