

���� A��BΪ������C��D�����������壬��DΪ����ɫ���壮�ס��ҡ���Ϊ�����Ļ�������Ǻ�ɫ�Ҿ��д��Ե����ʣ����ת����ϵ��֪����Ϊ������������BΪAl��AΪFe��CΪ��������Ϊƫ�����ƣ���Ϊ�Ȼ�����Ȼ����Ԫ�ػ�����֪ʶ����ѧ���������
��� �⣺A��BΪ������C��D�����������壬��DΪ����ɫ���壮�ס��ҡ���Ϊ�����Ļ�������Ǻ�ɫ�Ҿ��д��Ե����ʣ����ת����ϵ��֪����Ϊ������������BΪAl��AΪFe��CΪ��������Ϊƫ�����ƣ���Ϊ�Ȼ�����
��1��B���Ӧ�Ļ�ѧ����ʽΪ3Fe3O4+8Al$\frac{\underline{\;����\;}}{\;}$9Fe+4Al2O3��
�ʴ�Ϊ��3Fe3O4+8Al$\frac{\underline{\;����\;}}{\;}$9Fe+4Al2O3��
��2�������£���A��B�ĵ��ʷ���Ũ�����Ũ�����з����ۻ���������ȫ�ܽ⣬
�ʴ�Ϊ����
��3�����������ӵķ���Ϊȡ����������Һ���Թ��У��μ�KSCN��Һ������Һ��죬˵�����д���Fe3+��
�ʴ�Ϊ��ȡ����������Һ���Թ��У��μ�KSCN��Һ������Һ��죬˵�����д���Fe3+��
��4��A��ˮ������Ӧ����C�ͼĻ�ѧ����ʽΪ3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
�ʴ�Ϊ��3Fe+4H2O��g��$\frac{\underline{\;����\;}}{\;}$Fe3O4+4H2��
��5����B��NaOH��Һ��Ӧ�����ӷ���ʽ��2Al+2OH-+2H2O=2AlO2-+3H2�����������������ڱ�״����Ϊn L��n��H2��=$\frac{n}{22.4}$mol����n��Al��=$\frac{n}{22.4}$mol��$\frac{2}{3}$=$\frac{n}{33.6}$mol���ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����$\frac{n}{33.6}$��
����ȡ��ͬ�����ĸû��������м���������ϡ���ᣬ����ȫ���ܽ⣬�������������ڱ�״����Ϊm L��ת�Ƶ���Ϊ$\frac{m}{22.4}$��2����1-0��=$\frac{m}{11.2}$mol���������A������Ϊx���ɵ����غ��֪��$\frac{n}{33.6}$mol��3+$\frac{x}{56}$mol��2=$\frac{m}{22.4}$��2����1-0�������x=$\frac{m-n}{22.4}$��
�ʴ�Ϊ��$\frac{m}{11.2}$��$\frac{m-n}{22.4}$��
���� ���⿼��������ƶϣ�ע�����ȷ�Ӧ��DΪ����ɫ����Ϊ������ͻ�ƿڣ����ʵ��ƶ��ǽ����Ĺؼ��������еļ�����Ҫ�漰�����غ㼰��ϵʽ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ����� | 1��10-14 | �� | 1��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2���ӵĽṹʽ��O=C=O | |
| B�� | S2-�Ľṹʾ��ͼ�� | |
| C�� | R2+���Ӻ�����a�����ӣ�b�����ӣ�Rԭ�ӷ���Ϊ��${\;}_{a+2}^{a+b+2}$R | |
| D�� | ������ĵ���ʽ��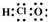 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
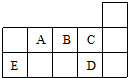
| A�� | ED4�����и�ԭ�Ӿ���8���ӽṹ | |
| B�� | AD3��ED4�����ӵ�����ԭ�Ӿ�Ϊsp3�ӻ� | |
| C�� | A��B��C��һ�����ܵĴ�С˳��ΪC��B��A | |
| D�� | C��D��̬�⻯���ȶ���ǿ���ͷе�ߵ;�ΪC��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol���к�������ĿΪ7NA | |
| B�� | ��״���£�22.4L�����й��ۼ���ĿΪ19NA | |
| C�� | 14g��ϩ�Ͷ�ϩ�Ļ�����к��е�ԭ������Ϊ3NA�� | |
| D�� | 1mol����ϩ��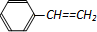 ���к��е�C=C��Ϊ4NA ���к��е�C=C��Ϊ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�۵ijɷ�Ϊ������ƣ��Ǵ����� | |
| B�� | ʵ���ҿ���Ũ������ﰱ�� | |
| C�� | ʵ���ҿ���NaOH��Һ����SO2��HCl���� | |
| D�� | ����Cl2��ʹ������ɫ������ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ��е�ˮ��CaO������ | B�� | �������е��Ҵ���ˮ����Һ�� | ||
| C�� | ���еļױ���Br2ˮ����Һ�� | D�� | �屽�е��壨NaOH��Һ����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
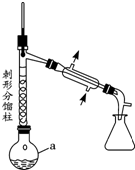 �����������н�����ʹ���ã��ǽ���ʹ�õĽ�����ʹҩ���С����ȱ���֮�ƣ����Ʊ�ԭ�����£�
�����������н�����ʹ���ã��ǽ���ʹ�õĽ�����ʹҩ���С����ȱ���֮�ƣ����Ʊ�ԭ�����£� NH2+CH3COOH$\stackrel{��}{?}$
NH2+CH3COOH$\stackrel{��}{?}$ NHCOOCH3+HO
NHCOOCH3+HO| ���� | �۵� | �е� | �ܽ�� |
| �������� | 114.3�� | 305�� | ������ˮ����������ˮ |
| ���� | -6�� | 184.4�� | ����ˮ |
| ���� | 16.6�� | 118�� | ������ˮ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com