
【题目】某兴趣小组拟制备氯气并验证其一系列性质.Ⅰ.【查阅资料】
①当溴水浓度较小时,溶液颜色与氯水相似也呈黄色.
②硫代硫酸钠溶液在工业上可作为脱氯剂.
(1)Ⅱ.【性质验证】实验装置如图1所示(省略夹持装置)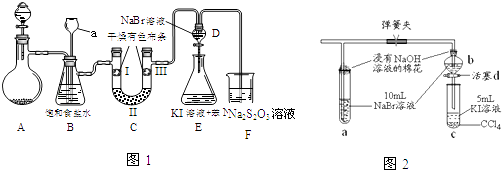
实验步骤:
a.检查装置气密性,按图2加入试剂.仪器a的名称是;装置CⅡ处加的试剂可以是(选填下列字母编号).
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
b.装置B的作用有 .
c.写出装置F中相应的离子反应方程式: .
(2)Ⅲ.【探究与反思】a.图1中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 . 该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
①打开弹簧夹,缓缓通入氯气
②当a和b中的溶液都变为黄色时,夹紧弹簧夹.
③当a中溶液由黄色变为棕色时,停止通氯气.
④ .
b.设计步骤③的实验思想是 .
c.步骤④的操作是 .
【答案】
(1)长颈漏斗;BD;除去氯气中的氯化氢并作安全瓶;S2O32﹣+4Cl2+5H2O=2SO42﹣+8Cl﹣+10H+
(2)未排除Cl2对溴、碘的非金属性的强弱实验的干扰;打开活塞d,将少量b中溶液滴入c中,关闭活塞d,取下试管c震荡;对比实验思想;打开活塞d,将少量b中溶液滴入c中,关闭活塞d,取下试管c震荡
【解析】解:(1)Ⅱ.a.仪器a的名称是长颈漏斗;装置CⅡ处加的试剂干燥氯气,且为固体,只有BD符合,所以答案是:长颈漏斗;BD;b.生成的氯气中混有HCl,则装置B的作用有除去氯气中的氯化氢并作安全瓶,所以答案是:除去氯气中的氯化氢并作安全瓶;c.Na2S2O3中硫显+2价,被氯气氧化SO42﹣ , 则装置F中相应的离子反应方程式S2O32﹣+4Cl2+5H2O=2SO42﹣+8Cl﹣+10H+ , 所以答案是:S2O32﹣+4Cl2+5H2O=2SO42﹣+8Cl﹣+10H+;(2)Ⅲ.a.装置D、E的目的是比较氯、溴、碘的非金属性,但氯气可与NaBr、KI均反应,未排除Cl2对溴、碘的非金属性的强弱实验的干扰,不能比较Cl、Br、I的非金属性,所以答案是:未排除Cl2对溴、碘的非金属性的强弱实验的干扰;b.设计步骤③的实验思想是对比实验思想,所以答案是:对比实验思想;c.改进的实验步骤④为打开活塞d,将少量b中溶液滴入c中,关闭活塞d,取下试管c震荡,第④步发生溴与KI的反应,所以答案是:打开活塞d,将少量b中溶液滴入c中,关闭活塞d,取下试管c震荡.
【考点精析】认真审题,首先需要了解氯气的化学性质(氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应).


科目:高中化学 来源: 题型:
【题目】1摩尔气态烃A最多和2摩尔HCl加成,生成氯代烷B,1摩尔B与4摩尔Cl2发生取代反应,生成只含碳、氯两种元素的C.则A的分子式为( )
A.C2H2
B.C2H4
C.C3H4
D.C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将Fe+2FeCl3=3FeCl2设计成原电池装置如图所示.下列说法正确的是( ) 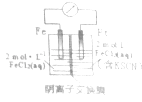
A.电子由铁极经溶液向铂极迁移
B.放电过程中交换膜右侧溶液颜色逐渐变浅
C.正极的电极反应式为Fe3++3e﹣=Fe
D.若转移2mole﹣ , 交换膜右侧溶液中约减少3mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的选项正确的是( )
A.配制0.10molL﹣1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2 , 分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述不正确的是( )
选项 | 已知 | 解释与结论 |
A | 活泼金属Al、不活泼金属Cu和浓硝酸可以形成原电池 | Al作正极,Cu作负极 |
B | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s) | 该反应的△H<0 |
C | 常温下,Ksp(AgCl)=1.8×10﹣10、 | 向BaCl2溶液中加入AgNO3和KBr,当AgCl、AgBr两种沉淀共存时, |
D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,振荡,溶液变为黄色 | 氧化性:H2O2>Fe3+ |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量浓度之比为( )
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列溶液的离子浓度关系正确的是( )
A.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合c(Na+)+c(H+)=c(OH﹣)+c( HC2O4﹣)
B.Na2S溶液:c(Na+)>c(HS﹣)>c(OH﹣)>c(H2S)
C.NaHSO4溶液:c(H+)=c(SO ![]() )十c(OH﹣)
)十c(OH﹣)
D.pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl﹣)>c(H+)>c(NH ![]() )>c(OH﹣)
)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用二氧化铈(CeO2)在太阳能的作用下将H2O、CO2转变成H2、CO。其过程如下:mCeO2![]() (m-x)CeO·xCe+xO2、(m-x)CeO2·xCe+xH2O+xCO2
(m-x)CeO·xCe+xO2、(m-x)CeO2·xCe+xH2O+xCO2![]() mCeO2+xH2+xCO。下列说法不正确的是
mCeO2+xH2+xCO。下列说法不正确的是
A. CeO2·xCe是该反应的催化剂 B. 该过程中CeO2没有消耗
C. 该过程实现了太阳能向化学能的转化 D. O2在第一个反应中作氧化产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com