
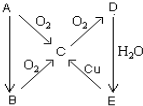
 A、B、C、D、E、在一定条件下的转换条件如图所示.
A、B、C、D、E、在一定条件下的转换条件如图所示.分析 根据题中各物质的转化关系,(1)若A在常温下为固态单质,C为能使品红溶液褪色的气体,即为SO2,则A为S,B为H2S,C为,D为SO3,E为浓硫酸,(2)若A在常温下为气态单质,则由转化关系可知,A为N2,B为NH3,C为NO,D为NO2,E为稀硝酸,以此来解答.
解答 解:根据题中各物质的转化关系,
(1)若A在常温下为固态单质,C为能使品红溶液褪色的气体,即为SO2,则A为S,B为H2S,C为,D为SO3,E为浓硫酸,
C→D变化的化学方程式为 2SO2+O2$?_{△}^{催化剂}$2SO3,
E→C变化的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:2SO2+O2$?_{△}^{催化剂}$2SO3;Cu+2H2SO4(浓)$\frac{\underline{\;△\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)若A在常温下为气态单质,则由转化关系可知,A为N2,B为NH3,C为NO,D为NO2,E为稀硝酸,A→B变化的化学方程式为N2+3H2$?_{催化剂}^{高温、高压}$2NH3,
故答案为:N2;NO2;N2+3H2$?_{催化剂}^{高温、高压}$2NH3.
点评 本题考查无机物的推断,为高频考点,把握物质的性质及相互转化为解答的关键,侧重N、S及其化合物性质的考查,注意连续氧化的特点,题目难度不大.


科目:高中化学 来源: 题型:解答题
 .
. 
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 金属离子 | PH值 | |
| 开始沉淀 | 完全沉淀 | |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.4 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电化学原理在医学医疗中有重要应用.
电化学原理在医学医疗中有重要应用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
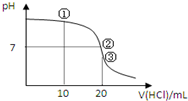 常温下,用0.1000mol/L HCl溶液滴定20.00mL 0.1000mol/L NH3•H2O溶液,滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol/L HCl溶液滴定20.00mL 0.1000mol/L NH3•H2O溶液,滴定曲线如图.下列说法正确的是( )| A. | ①溶液:c(C1-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | ②溶液:c(NH4+)>c(C1-)>c(OH-)=c(H+) | |
| C. | ③溶液:c(H+)>c(NH3•H2O)+c(OH-) | |
| D. | 滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 物质 | 试剂 | 除杂方法 |
| ① | 甲烷(C2H4) | ||
| ② | 硝基苯(混合酸) | ||
| ③ | KNO3(NaCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
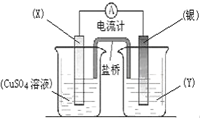 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 CO(g)+H2(g).
CO(g)+H2(g).| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com