
【题目】常温下,用0.10 mol/L的NaOH溶液分别滴定体积均为50.00 mL、浓度均为0.05 mol/L的HClO、HF两种溶液,其滴定曲线如图所示。

下列说法正确的是
A.HClO的酸性比HF强
B.V(NaOH)=0mL时,对应溶液中:c(ClO-)=c(F-)
C.V(NaOH)=12.50mL时,对应溶液中:c(ClO-)>c(F-)
D.V(NaOH)=25.00mL时,对应溶液中:c(ClO-)<c(F-)
【答案】D
【解析】
A.浓度均为0.05 mo1/L的HClO、HF,溶液的pH越小,酸的酸性越强,滴定前HF的pH小,所以酸性HF>HClO,A错误;
B.电离程度越大,溶液中酸根离子的浓度越大,滴定前,HF中酸根离子浓度大,即c(ClO-)<c(F-),B错误;
C.V(NaOH)=12.50mL时,溶液中溶质分别为等浓度的NaClO和HClO、NaF和HF,由于HF的电离程度大于HClO,所以对应溶液中:c(ClO-)<c(F-),C错误;
D.V(NaOH)=25.00mL时,两种溶液中的溶质分别为等浓度的NaClO、NaF,由于NaClO的水解程度大于NaF,所以c(ClO-)<c(F-),D正确;
故合理选项是D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】洁净安全的生存环境:2012年3月,新《环境空气质量标准》的颁布表明国家对环境问题的进一步重视。
(1)煤燃烧产生的SO2所形成的酸雨中,SO2最终转化成的酸是___(填化学式)。在煤中加入适量___,可以大大减少煤燃烧时SO2的排放,该反应的化学方程式为:___。
(2)A、B、C三个城市全年雨水的月平均pH变化如图所示。
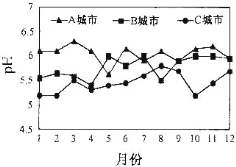
①受酸雨危害最严重的是___城市。
②汽车尾气中含有NO2、NO、CO等有害气体。汽车安装尾气净化装置可将NO、CO转化为无害气体。写出该反应的化学方程式:___。
③自来水生产过程中要经过:去除固体杂质和悬浮物、消毒、去除异味等一系净化工序。天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用:加入ClO2的作用是___;加入明矾后,Al3+水解生成的___(填化学式)胶体能吸附水中的悬浮颗粒,并使之沉降。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)该反应的化学方程式为______。
(2)反应开始至2min,以气体Z表示的平均反应速率为______。平衡时X的转化率为______。
(3)2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时______![]() 填“大”、“小”或“相等”,下同
填“大”、“小”或“相等”,下同![]() ,混合气体密度比起始时______。
,混合气体密度比起始时______。
(4)下列叙述能证明该反应已经达到化学平衡状态的是![]() 填序号
填序号![]() ______。
______。
A.Y的体积分数不再变化 B.容器内气体压强不再变化
C.υ(X) :υ(Y) =3:1 D.单位时间内消耗3nmol X同时生成2nmol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( )

A. 三种酸的电离常数关系:KHA>KHB>KHD
B. 滴定至P点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
C. pH=7时,三种溶液中:c(A-)=c(B-)=c(D-)
D. 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c)表示止水夹。

请按要求填空:(可供选择的试剂有:Cu片,MnO2粉末,浓硝酸,稀硝酸,浓硫酸,浓盐酸,氢氧化钠溶液,酚酞)
(1)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。若在丙中加入适量水,即可制得氯水。将所得氯水加入到滴有酚酞的NaOH溶液中,观察到溶液褪色,甲同学给出的结论是氯水溶于水生成了酸,将NaOH中和后溶液褪色。
a.写出制取氯气的化学方程式:___。
b.乙同学认为甲同学的结论不正确,他认为褪色的原因可能是___。
c.如何验证甲、乙两同学的结论(写出所加试剂,现象,结论):___。
(2)B、D、E装置相连后,可制得NO2并进行有关实验。
①B中发生反应的化学方程式为___。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹___,再打开止水夹___,使烧杯中的水进入试管丁的操作是___。
③试管丁中的NO2与水充分反应,若向试管内缓缓通入一定量的O2,直到试管全部充满水,则所得溶液中的溶质的物质的量浓度是___(气体按标准状况计算,结果保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氯碱工业的简易装置示意图,其中两电极均为惰性电极,下列说法正确的是
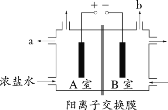
A.粗盐水中含有的少量 Ca2+和 Mg2+均可用 NaOH 除去
B.若电路中通过 0.2 mol 电子,理论上可在 b 处得到标准状况下 1.12 L 气体
C.a 处得到的是浓 NaOH 溶液
D.适当降低阳极电解液的 pH 有利于 Cl2 逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将淀粉水解并用新制Cu(OH)2悬浊液检验水解产物的实验中,要进行的主要操作有:①加热;②滴入稀硫酸;③加入新制的Cu(OH)2悬浊液;④加入NaOH溶液中和。以上各步操作的先后顺序排列正确的是________。
A.②③④① B.②④③① C.②①④③ D.④③②①
(2)若某学生称取9g淀粉溶于水,按以下步骤做淀粉水解实验,回答下列问题。

①写出淀粉水解的化学方程式:________________。
②沉淀的单质是________________(写化学式)。
③填写所加试剂名称及其作用:
A________,作用________________________________;
B________,作用________________________________。
④当析出3.24g单质沉淀时,淀粉的水解率为________(已知1mol醛基发生银镜反应时生成2molAg)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L盐酸分别滴定10.00 mL浓度均为0.1000 mol/L的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O]=1.6×10-4),利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是( )

A.盐酸滴定二甲胺实验中选择酚酞做指示剂比选甲基橙误差更小
B.d点溶液中:c(H+)<c(OH-)+c[(CH3)2NH2+]
C.a点溶液与d点的溶液混合后的溶液中:c[(CH3)2NH2+]<c[(CH3)2NH·H2O]
D.b、c、e三点的溶液中,水的电离程度最大的是e点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,在充电和放电时,其电池反应为Mg+2MnF3![]() 2MnF2+MgF2。下列说法不正确的是( )
2MnF2+MgF2。下列说法不正确的是( )
A. 放电时,镁为负极材料
B. 放电时,电子从镁极流出,经电解质流向正极
C. 充电时,阳极的电极反应式为:MnF2+F--e-=MnF3
D. 充电时,外加直流电源负极应与原电池的Mg极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com