
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年安徽省淮北市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列有关粒子组的评价及相关离子方程式均正确的是
选项 | 粒子组 | 评价及离子方程式 |
A | K+、Al3+、 SO42-、NO3- | 能大量共存于同一溶液中 |
B | H+、CH3CHO、SO42-、MnO4- | 能大量共存于同一溶液中 |
C | NH4+、Fe3+、SCN-、Cl- | 不能大量共存,Fe3+ +3SCN- = Fe(SCN)3↓ |
D | Na+、K+、HCO3-、OH- | 不能大量共存,HCO3- + OH- = H2O + CO2↑ |
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下表给出几种物质的熔点,对此有下列一些说法:
物质 | SiO2 | MgCl2 | CaCl2 | SiCl4 |
熔点(℃) | 1723 | 712 | 782 | -68 |
①CaCl2属于离子晶体
②SiCl4是分子晶体
③一个SiO2分子由1个Si原子和2个O原子构成
④MgCl2在熔化状态不能导电
上述说法中正确的有
A.仅① B.①和② C.仅② D.①、②和③
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
A、B、C、D为四种短周期元素,已知A、C同主族,B、D同周期, A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;若B的阳离子比C的阴离子少一个电子层, 下列叙述正确的是
A.原子序数:A>B>D>C B.金属性B>D,非金属性A>C
C.原子半径:D>B>C>A D.简单离子半径:C>B>D>A
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列变化中既有离子键断裂,又有共价键断裂的是
A.NaCl溶于水 B.HCl溶于水
C.干冰气化 D.KClO3受热分解
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北武汉市高三毕业生四月调研测试理综化学试卷(解析版) 题型:填空题
(15分)合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) == 2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。

结合①中信息,尿素还原NO(g)的热化学方程式是 。
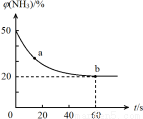
②密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) ==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中离子浓度大小关系是c(Na+)>______。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北武汉市高三毕业生四月调研测试理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.测定酸碱滴定曲线实验所用玻璃仪器有酸式滴定管、碱式滴定管、锥形瓶、烧杯
B.除去乙酸乙酯中混有的乙酸采用加入饱和NaOH溶液后进行分液的方法
C.除去粗盐中不溶性杂质的操作有溶解、过滤、蒸发
D.石蜡油蒸气在炽热碎瓷片的作用下分解产生的气体可使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三4月模拟考试理综化学试卷(解析版) 题型:简答题
(16分)制备多晶硅(硅单质的一种)的副产物以SiCl4为主,其对环境污染很大,遇水强烈水解,放出大量热量。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成份为BaCO3,含有钙、铁、镁等离子)制备BaCl2·2H2O,流程为:
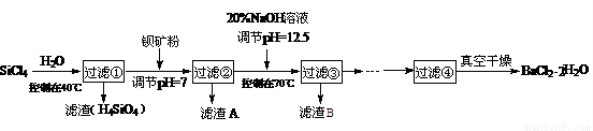
已知常温下Fe3+、Mg2+完全沉淀的pH分别是3.4和12.4;
(1)①SiCl4水解控制在40℃以下的原因是 。
②已知:SiCl4(s)+H2(g)=SiHCl3(s)+HCl(g) ΔH1=47 kJ/mol
SiHCl3(s)+H2(g)=Si(s)+3HCl(g) ΔH2=189 kJ/mol
则SiCl4被H2还原制备硅的热化学方程式 。
(2)加钡矿粉时生成BaCl2的离子反应方程式 。
(3)过滤②的滤渣A的成分化学式为 ;接着往滤液中加20% NaOH调节pH=12.5,控制温度70℃时,滤渣B的主要成分的化学式 ,控制温度70℃的目的 。
(4)滤液③经 、过滤等操作,再经真空干燥后得到BaCl2·2H2O。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用的叙述都正确的是
A.明矾溶液具有强氧化性,可用作净水剂
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀
D.常温下,铝能被浓硝酸钝化,可用铝制槽车运送浓硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com