


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
 将红热固体单质甲放在显黄色的溶液乙中剧烈反应,产生混合气体A,A在常温下(不与空气接触)有如下变化:
将红热固体单质甲放在显黄色的溶液乙中剧烈反应,产生混合气体A,A在常温下(不与空气接触)有如下变化:查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示:
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
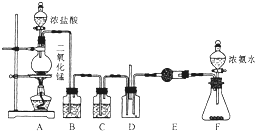 某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应.其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置.
某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应.其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 水杨酸具有防腐杀菌作用,还有祛除汗臭、止痒消肿、止痛消炎等功能,主要用于花露水、痱子水以及一些水类化妆品.水杨酸的结构简式如图所示,请回答下列问题.
水杨酸具有防腐杀菌作用,还有祛除汗臭、止痒消肿、止痛消炎等功能,主要用于花露水、痱子水以及一些水类化妆品.水杨酸的结构简式如图所示,请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com