
����˵����ȷ����
| A����п�����������������������������������ﵽ��ֹ��ʴ��Ŀ�� |
| B���ڵ��з�̪��Na2CO3��Һ�У�����BaCl2��Һ���ɫ��ȥ��˵��BaCl2��Һ������ |
| C���ϳɰ���Ӧ��ʹ�ô�����˵���������Դٽ���ƽ�������ɰ��ķ����ƶ� |
D������β���ľ�����Ӧ2NO��2CO 2CO2��N2��H��0����÷�Ӧһ�����Է����� 2CO2��N2��H��0����÷�Ӧһ�����Է����� |
A
�������������A��п�������ã����Զ�п���屻��ʴʱ��п��ʧ���ӱ���ʴ���Ӷ��������������ַ�����Ϊ������������������������ȷ��B������BaCl2��Һ���ɫ��ȥ������Ϊ��������̼������ӽ�ϳ�̼�ᱵ������ʹ̼������ӵ�ˮ��ƽ�������ƶ�����Һ��������ֱ��Ϊ���ԣ���ɫ��ʧ����Ϊ��C����Ӧ�м��������ֻ�ܼӿ췴Ӧ���ʣ������ܸı�ƽ����ƶ�����Ϊ��D���ʼ�������Ӧһ���Է����У����÷�Ӧ�ġ�H��0����S<0�����Է�Ӧ��һ���Է�������ѡA��
���㣺��������ķ�����ˮ��ƽ���Ӧ�ã�������ƽ���Ӱ�죬��Ӧ�Է����ж�


 ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д� �����Ծ�ϵ�д�
�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����Һ�������25�棬�й�������ȷ����
| A��ij���ʵ���ҺpH <7���������һ�������ǿ�������� |
| B���ù㷺pH��ֽ���0.10 mol��L��1 NH4Cl��Һ��pH��5. 2 |
| C��pH=2��CH3COOH��c(H+)��pH=1��CH3COOH��c(H+)��2�� |
| D��AgCl����ͬ���ʵ���Ũ�ȵ�CaCl2��HCl��Һ�е�Ksp��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪Ksp(AgCl)=1��56��10-10��Ksp(AgBr)=7��7��10-13��Ksp(Ag2CrO4)=9��0��10-12��ij��Һ�к���Cl-��Br-��CrO42-��Ũ�Ⱦ�Ϊ0��010mol?L-1�������Һ����μ���0��010 mol?L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
| A��Cl-��Br-��CrO42- | B��CrO42-��Br-��Cl- | C��Br-��Cl-��CrO42- | D��Br-��CrO42-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ��������ɵ�������AC��BD��AD��BC��Ϊ0.1 mol��L��Һ����ͬ���£�ǰ������ҺpH��7����������ҺpH��7�����һ����ҺpH��7�� ���γ������ε���ͼ�ǿ���Ƚ���ȷ����
| | A | B | C | D |
| �� �� | AOH��BOH | AOH��BOH | AOH��BOH | AOH��BOH |
| �� �� | HC��HD | HC��HD | HC��HD | HC�� HD |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£����и���Һ����������ȷ����
| A��NaHSO3��Na2SO3�����Һ�У�3c(Na+) = c(HSO3-) + c(SO32-) |
| B��0.1mol��L-1�Ĵ�������Һ20 mL��0.1mol��L-1����10 mL��Ϻ���Һ������ c (CH3COO-)��c (Cl-)��c (CH3COOH)��c (H+) |
| C�������ʵ���Ũ�ȵ������NH4HSO4��NaOH��Һ��ϣ� c(Na+)��c(SO42-)��c(NH4+)��c(H+)��c(OH-) |
| D����1.00 L 0.3mol��L-1NaOH��Һ�л���ͨ��0.2molCO2���壬��Һ�У� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ�и����ӵ�Ũ�ȹ�ϵ����ȷ����(����)
| A��0��1 mol��L��1CH3COONa��Һ�У�c(CH3COO��)��c(CH3COOH)��0��1 mol��L��1 |
| B��Ũ�Ⱦ�Ϊ0��1 mol��L��1 Na2CO3��Һ��ϡ����������Ϻ����Һ�У� c(CO 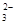 )��c(OH��)��c(H��)��c(H2CO3) )��c(OH��)��c(H��)��c(H2CO3) |
| C��25 ��ʱ��pH��9��4��Ũ�Ⱦ�Ϊ0��1 mol��L��1��HCN��NaCN�Ļ����Һ�У� c(Na��>c(CN��)>c(HCN)>c(OH��) |
| D�� 3��0 L 0��1 mol��L��1 NaOH��Һ�л���ͨ��CO2����Һ����8��8 gʱ����Һ�У� |
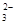 )>c(HCO
)>c(HCO )>c(OH��)>c(H��)
)>c(OH��)>c(H��)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ�����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����
| A��0.1mol/LNaHCO3��Һ��0.1mol/LNaOH��Һ�������ϣ�������Һ�У� c(Na��)��c(CO32��)��c(HCO3��)��c(OH��) |
| B��20ml0.1mol/LCH3COONa��Һ��10ml0.1mol/LHCl��Һ��Ϻ�����ԣ�������Һ�У� c(CH3COO��)��c(Cl��)��c(CH3COOH)��c(H��) |
| C�������£�pH��2��������pH��12�İ�ˮ�������ϣ�������Һ�У� c(Cl��)��c(H��)��c(NH4��)��c(OH��) |
| D��0.1mol/LCH3COOH��Һ��0.1mol/LNaOH��Һ�������ϣ�������Һ�У� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪ij�¶���CH3COOH��NH3?H2O �ĵ��볣����ȣ�����10mLŨ��Ϊ0.1mol?L?1��CH3COOH��Һ�еμ���ͬŨ�ȵİ�ˮ���ڵμӹ�����
| A��ˮ�ĵ���̶�ʼ������ |
| B��c��NH4+��/c��NH3?H2O���������ټ�С |
| C��c��CH3COOH����c��CH3COO?��֮��ʼ�ձ��ֲ��� |
| D�������백ˮ�����Ϊ10mLʱ��c(NH4+)=c(CH3COO?) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
25��ʱ��������(HA)������(NaA)��ɵĻ����Һ����ʼŨ�Ⱦ�Ϊ1mol��L-1����ͼΪ�����Һ��ͨ��HCl��������NaOH����ʱ����ҺpH�����H+��OH-�����ʵ������仯�����ߡ�����˵���У���ȷ����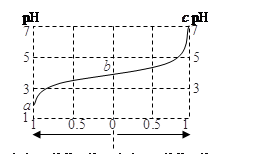
A����NaOH��HA����ƽ�ⳣ������
B��ͨ��HCl����Һ��������Ũ��֮�ͼ�С
C����Һ��ˮ�ĵ���̶�a��b��c
D��b����Һ�У�c(HA)��c(A-)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com