
����Ŀ���������Һ����������ϢϢ��أ���ش���������
��1��ij�¶��£�Kw=1��10��12�� molL��1��2 �� �������¶Ȳ��䣬��ˮ�е���ϡ����ǡ��ʹ��Һ��c��H+��/c��OH����=1��1010 �� ���ʱˮ�������c��H+��=molL��1 ��
��2������������Һ��pH=3��HA��ҺV1 mL��pH=11��NaOH��ҺV2 mL��϶��ã�������˵����ȷ���� ��
A.����Ϻ���Һ�����ԣ���c��H+��+c��OH����=2��10��7mol/L
B.��V1=V2 �� ��Ϻ���Һ��pHһ������7
C.����Ϻ���Һ�����ԣ���V1һ������V2
D.����Ϻ���Һ�ʼ��ԣ���V1һ��С��V2
��3�����������У������������ᣨ�ף�Ka=1.8��10��5 mol/L����һ�����ᣨ�ң�Ka=1.4��10��3 mol/L����ˮ�еĵ������Ũ�ȹ�ϵ���� �� 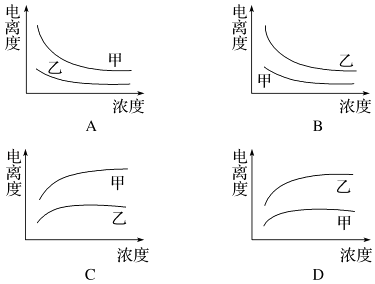
��4��������ʵ���У���֤���������Ա��������������� ��
A.���������pH=4������ʹ���ϡ�ͳ�pH=5����Һ�������������ˮ���Ķ���
B.����������pH������ʹ����зֱ����ͬ������Ӧ���ι��壬����Һ��pH���ޱ仯
C.����������Ũ�ȵ�����ʹ���ֱ��������п�ۣ������������������
D.�õ��������Ũ�ȵ�����ʹ�����������ʵ�飬���ݵ��ݵ������̶ȣ�
���𰸡�
��1��10��11
��2��A,D
��3��B
��4��A,B,D
���������⣺��1��ij�¶��£�Kw=1��10��12�� molL��1��2�����¶���ˮ�м���ϡ�������Һ�д���c��H+��/c��OH����=1��1010������Һ��c��H+��=0.1mol/L������Һ��ˮ�������c��OH����= ![]() mol/L=10��11 mol/L������Һ��ˮ�������c��H+��������Һ��c��OH����=10��11 mol/L��
mol/L=10��11 mol/L������Һ��ˮ�������c��H+��������Һ��c��OH����=10��11 mol/L��
��2��pH=3��HA��Һ�У�c��HA����0.001mol/L��pH=11��NaOH��Һ��c��NaOH��=0.001mol/L��
A������ҺM�����ԣ���c��H+��=c��OH����=1��10��7molL��1����c��H+��+c��OH����=2��10��7molL��1����A��ȷ��
B����V1=V2������HA��ǿ��δ֪����Ӧ����Һ������Բ���ȷ������ҺM��pH��һ������7����B����
C����HAΪ���ᣬ�������ϣ���ҺҲ���ܳ����ԣ���V1��һ������V2����C����
D����HAΪ���ᣬ�������ϳ����ԣ���ʼ��ԣ�V1һ��С��V2����HAΪǿ�ᣬ��Ӧ��ʼ��ԣ���V1һ��С��V2����D��ȷ��
��3�������ᣨ�ס�Ka=1.8��10��5����һ�����ᣨ�ҡ�Ka=1.4��10��3����֪�������KaС�����������������
��ͼ��֪��������ΪŨ�ȣ�������Ϊ����ȣ����Ũ��ʱ����ǿ�ĵ���ȴ��ҵ��������Ϸ������ų�A��C��
�����Ũ��Խ��������ԽС�������ס��Ҿ���Ũ�ȵ�������½������ų�D����Ȼֻ��B���ϣ�
��4��A�����������pH=4������ʹ���ϡ�ͳ�pH=5����Һ�������������ˮ���Ķ��٣���������ˮ���������ᣬ˵�������д��ڵ���ƽ�⣬���������С�����ᣬ��Aѡ��
B������������pH������ʹ����зֱ����ͬ������Ӧ���ι��壬����Һ��pH���ޱ仯�����������ƴ�����뵼������ҺpH������֤����������С�����ᣬ��Bѡ��
C������������Ũ�ȵ�����ʹ���ֱ��������п�ۣ����������������������������������������ʵ��������ȣ�������ǿ���أ����Բ���֤����������С�����ᣬ��C��ѡ��
D���õ��������Ũ�ȵ�����ʹ�����������ʵ�飬���ݵ��ݵ������̶�ȷ����Һ������Ũ�ȣ��Ӷ�ȷ������ǿ������Dѡ��
���Դ��ǣ���1��1��10��11����2��AD����3��B����4��ABD


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NaHSO2��Һ�ڲ�ͬ�¶��¾��ɱ�����KlO3��������NaHSO3��ȫ���ļ���I2����������I2��������ʱ��������NaHSO3�ķ�Ӧ���ʣ���Ũ�Ⱦ�Ϊ0.020 molL��1��NaHSO3��Һ�����������ۣ�10.0 mL��KIO3��������������Һ40.0 mL��ϣ���¼10��55�����Һ����ʱ�䣬55��ʱδ�۲쵽��Һ������ʵ������ͼ����ͼ�����������жϲ���ȷ���ǣ�������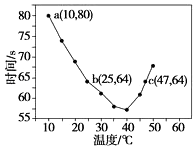
A.40��֮ǰ��40��֮����Һ������ʱ�����¶ȵı仯�����෴
B.ͼ��a���Ӧ��NaHSO3��Ӧ����Ϊ5.0��10��5 molL��1s��1
C.ͼ��b��c�����Ӧ��NaHSO3��Ӧ�������
D.40��֮���۲���������ʵ���ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̲��漰��ѧ�仯����
A.������ʳ��ƾ����˵��������������Ҵ��ı仯����
B.��������ˮ�����ã���ˮ��ɫ
C.ֲ�����⻯�õ�����֬��
D.����ȼ�ϵ�طŵ�ʱ��ѧ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦC��s��+H2O��g��H2��g��+CO��g������H��0�ﵽƽ��ı�ijһ������������ı����ʵ����������£�����Ӧ����v��ʱ��t�Ĺ�ϵ��ͼ��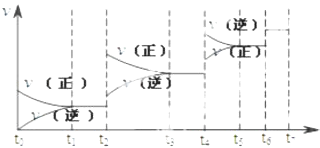
��ͼ��t2��t3�Ρ�t4��t6��ʱ����ƽ���ƶ��������ֱ����������
��ͼ�б�ʾƽ��������CO�ĺ�����ߵ�һ��ʱ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ؾ���(K3[Fe(C2O4)3]��3H2O)������ˮ���������Ҵ����������Թ����У������¼������ֽ⡣���������������Ʊ�����������������и��⣺

��1���ܽ�ʱ��ϡ�����������__________________________
��2�����ܽ�Һ����һ�����IJ��������У��γɻ�ɫ���������ˣ�ϴ�ӡ�
������ͼ�ǹ���װ��ͼ��ָ��ͼ���������Դ���һ����_____________________����һ����©�����¼��û�н������ܵ��ձ���

�����ȷ�������Ѿ�ϴ�Ӹɾ�____________________________________��
��3�����������г����Ͻ����⣬ά���¶���40�����ң�ԭ����___________________________��
��4��д�������������������������ص����ӷ���ʽ__________________________________��
��5�����������������ؾ�������¼��ɷֽ��������ֲ����Ρ�CO2�ȡ�д���÷ֽⷴӦ�Ļ�ѧ����ʽ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ����������ԭ��Ӧ�Ļ�ѧ��Ӧ���ʵ���
A. C��s��+ CO2 ![]() 2CO��Ӧ�У�����C����
2CO��Ӧ�У�����C����
B. ��ϡH2SO4��Ϊ98%��ŨH2SO4��Zn��Ӧ��ȡH2
C. ��H2SO4��NaOH����Һ��Ӧʱ������ѹǿ
D. ���º��������£��ڹ�ҵ�ϳɰ���Ӧ�У����ӵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʳƷ��ȫ�¹�Ƶ�����������Ƕ�ʳƷ���Ӽ�����ʶ���Butylated Hydroxy Toluene�����BHT����һ�ֳ��õ�ʳƷ�����������ϳɷ������������֣�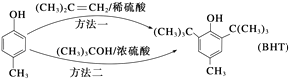
����˵����ȷ���ǣ�������
A.![]() ����Na2CO3��Һ��Ӧ����CO2
����Na2CO3��Һ��Ӧ����CO2
B.![]() ��BHT��Ϊͬϵ��
��BHT��Ϊͬϵ��
C.BHT�����ڿ����в��ᱻ����
D.���ַ����ķ�Ӧ���Ͷ��Ǽӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص���ʽ����д��ȷ����( )
A. N2 �ĵ���ʽ��![]() B. NH4Cl �ĵ���ʽ��
B. NH4Cl �ĵ���ʽ��
C. HClO �ĵ���ʽ��![]() D. CO2 �ĵ���ʽ��
D. CO2 �ĵ���ʽ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ع�˾���������Ƶ����һ���Խ�����Ϊ��������Ϊ�������մɹ�Ϊ����ʸ�Ĥ(�����Ǵ���Na+)�Ķ��ε�أ���ԭ�����Ա�ʾΪ2Na+xS![]() Na2Sx���ֽ��õ�����ڵ縡ѡ���۷�����ˮ���д�������Դ�����ֱ�����Fe�缫��ʯī�缫������ˮ���д�������Һ�ϲ��д����ĸ����������й�˵���������
Na2Sx���ֽ��õ�����ڵ縡ѡ���۷�����ˮ���д�������Դ�����ֱ�����Fe�缫��ʯī�缫������ˮ���д�������Һ�ϲ��д����ĸ����������й�˵���������

A. ���Ƶ�طŵ�ʱ������Ӧ����ʽ�ɱ�ʾΪ:xS+2e-+2Na+=Na2Sx
B. Fe�缫Ϊ����������ʧ���������������ӣ����ջ�ת��Ϊ�������γ�������������Ӷ��ﵽ��ˮĿ��
C. ������ˮʱ��������������ɽ�ˮ�е����������ˮ���γɸ����㣬����ѡ����
D. ���Ƶ�س��ʱ�������������ƶ���ÿ����1molNaת��xmol����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com