
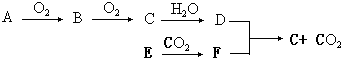
���� ����D��һ��ǿ�ᣬA��������Ӧ����B��B��������Ӧ����C��˵��BCΪ�����A�����Ƿǽ������ʣ�Ҳ�����Ƿǽ����⻯�E��һ�ֳ����������С��������������������ж�ΪMg������CO2��ȼ������MgO��C��F����D����������C�Ͷ�����̼����̼����ķ�Ӧ��Ũ�����Ũ���ᶼ���Է�Ӧ�������ɵIJ��Ǻ�����Ԫ�ػ��ϼ���ͬ������֤��DΪ���ᣬŨ������ϣ��ж�AΪN2��NH3��BΪNO��CΪNO2��DΪHNO3��EΪMg��FΪC��
��1������������֪DΪ���ᣬ��AΪ����������
��2��E��CO2��ȼ�յķ�ӦΪMg�Ͷ�����̼��Ӧ����̼������þ��
��3��D��F�ķ�Ӧ��̼��Ũ������ȵķ�Ӧ���ɶ�����̼������������ˮ���������ǿ�����ԣ�
��4�����������ͭ��Ӧ��ʼ���ɶ����������������һ��������
��� �⣺����D��һ��ǿ�ᣬA��������Ӧ����B��B��������Ӧ����C��˵��BCΪ�����A�����Ƿǽ������ʣ�Ҳ�����Ƿǽ����⻯�E��һ�ֳ����������С��������������������ж�ΪMg������CO2��ȼ������MgO��C��F����D����������C�Ͷ�����̼����̼����ķ�Ӧ��Ũ�����Ũ���ᶼ���Է�Ӧ�������ɵIJ��Ǻ�����Ԫ�ػ��ϼ���ͬ������֤��DΪ���ᣬŨ������ϣ��ж�AΪN2��NH3��BΪNO��CΪNO2��DΪHNO3��EΪMg��FΪC��
��1������������֪DΪ���ᣬ��AΪ������������ѧʽΪ��N2��NH3��
�ʴ�Ϊ��N2��NH3��
��2��E��CO2��ȼ�յķ�ӦΪMg�Ͷ�����̼��Ӧ����̼������þ����Ӧ�Ļ�ѧ����ʽΪ��2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
�ʴ�Ϊ��2Mg+CO2$\frac{\underline{\;��ȼ\;}}{\;}$2MgO+C��
��3��D��F�ķ�Ӧ��̼��Ũ������ȵķ�Ӧ���ɶ�����̼������������ˮ���������ǿ�����ԣ���Ӧ�Ļ�ѧ����ʽΪ��C+4HNO3$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+NO2��+2H2O����������������ԣ�
�ʴ�Ϊ��C+4HNO3$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+NO2��+2H2O�������ԣ�
��4������D����Һ����������Һ�м���������ͭ��50mL14mol•L-1����D���������Һ�У��������ʵ����ʵ���Ϊ0.7mol����ַ�Ӧ���ռ������壨NO2��NO��2.24L����״���£�����ԭ������Ϊ0.1mol�������ͭ���ӽ�ϵ������Ϊ0.6mol���μӷ�Ӧ��ͭΪ0.3mol������Ϊ0.3mol��64g/mol=19.2g��
�ʴ�Ϊ��0.1��19.2��
���� �����Կ�ͼ����ʽ���������ƶϣ�Ϊ�߿��������ͣ�������ѧ���ķ��������ͼ��������Ŀ��飬�漰��Ԫ�ػ��������ʵȣ����ʵ��������ʼ�����ת����ϵ���ƶ�ͻ�ƿڣ����ضԻ���֪ʶ���̣��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
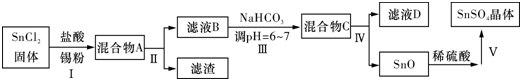
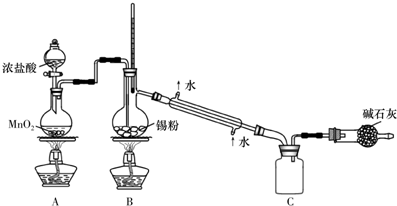
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KClO3�ڷ�Ӧ���ǻ�ԭ�� | |
| B�� | 1molKClO3�μӷ�Ӧ���ڱ�״�����ܵõ�22.4L���� | |
| C�� | ��Ӧ��H2C2O4�Ȳ���������Ҳ���ǻ�ԭ�� | |
| D�� | 1molKClO3�μӷ�Ӧ��1mol����ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.7g OH- ����������Ϊ0.9NA | |
| B�� | ��״���£�11.2 L HCl ����������Ϊ18NA | |
| C�� | �����£�11.2 L Cl2 ������ԭ����ΪNA | |
| D�� | 0.5 mol D2O ������������Ϊ5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+��SO42-��NO3-��Ba2+ | B�� | K+��Cl-��CO32-��Na+ | ||
| C�� | Cu2+��NO3-��OH-��Na+ | D�� | K+��SO42-��HCO3-��H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/s | 0 | 50 | 150 | 250 | 350 |
| n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A�� | ��Ӧ��ǰ50s ��ƽ������ ��PCl3��=0.0032mol•L-1•s-1 | |
| B�� | ���������������䣬�����¶ȣ�ƽ��ʱ ��PCl3��=0.11mol•L-1����Ӧ�ġ�H��0 | |
| C�� | ��ͬ�¶��£���ʼʱ�������г���1.0mol PCl5��0.20mol PCl3��0.20mol Cl2����Ӧ�ﵽƽ��ǰ �����������棩 | |
| D�� | ��ͬ�¶��£���ʼʱ�������г���2.0mol PCl3��2.0mol Cl2���ﵽƽ��ʱ��PCl3��ת����С��80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯī����ʯ | B�� | 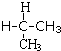 �� �� 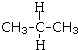 | C�� |  �� �� 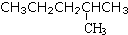 | D�� | 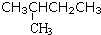 �� ��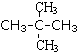 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com