
| A. | 1 mol氢气含有的原子数为NA | |
| B. | NA个水分子中含有氢原子的物质的量为2 mol | |
| C. | 1 mol 氧气中含有的分子数为2NA | |
| D. | 1 mol任何物质都含有NA个分子 |
分析 A、根据分子个数N=nNA来计算,而氢气是双原子分子;
B、NA个水分子的物质的量为1mol,中含有氢原子的物质的量为2 mol;
C、根据分子个数N=nNA来计算;
D、物质构成可以是分子、原子、离子.
解答 解:A、1mol氢气中含有的氢原子个数N=2nNA=2NA个,故A错误;
B、NA个水分子的物质的量为1mol,中含有氢原子的物质的量为2 mol,故B正确;
C、1 mol 氧气中含有的分子数为NA,故C错误;
D、物质构成可以是分子、原子、离子,1mol任何物质都含有6.02×1023个构成微粒,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 向溶液中加入适量NaA固体,若溶液pH不变,则HA为强酸 | |
| B. | 若HA为弱酸,则该溶液导电能力比等体积pH=5的盐酸弱得多 | |
| C. | 若HA为弱酸,则加入等体积pH=9的NaOH溶液,所得溶液pH>7 | |
| D. | 取该溶液1.00mL,加水稀释至1000mL,所得溶液pH=8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
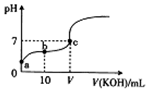 已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )
已知25℃时CH3COOH的电离常数K=1.6×10-5.该温度下向20ml 0.01mol•L-1 CH3COOH溶液中逐滴加入0.01mol•L-1 KOH溶液,其pH变化曲线如图所示(忽略温度变化),下列有关叙述正确的是 ( )| A. | a点溶液中c(H+)为4.0×10-5mol/L | |
| B. | c点溶液中的离子浓度大小顺序为c(K+)>c(CH3COO-)>c(H+)=c(OH-) | |
| C. | V=20 | |
| D. | a、b、c三点中水的电离程度最大的是c点 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
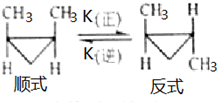 顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如图转化:
顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如图转化:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 难容电解质 | AgCl | AgBr | Agl | Ag2SO4 | Ag2CrO4 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 8.5×10 -17 | 1.4×10-5 | 1.12×10-12 |
| A. | 由溶度积常数可以判断相应物质的溶解性大小 | |
| B. | 将等体积的 4×10-3 mol/L 的 AgNO3 溶液和 4×10-3 mol/L K2CrO4溶液混合,有 Ag2CrO4沉淀产生 | |
| C. | 向 AgCl 的悬浊液中滴加饱和 NaBr 溶液不能得到黄色 AgBr | |
| D. | 向 100 mL 0.02mol/L 的 NaSO4 溶液中加入 100mL0.02mol/L 的 AgNO3 溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Z、Y、X、W的原子序数依次减小 | |
| B. | W与X可形成既含极性共价键又含非极性共价键的化合物 | |
| C. | Z的最高价氧化物对应的水化物是短周期元素形成的最强碱 | |
| D. | X的简单氢化物的沸点低于Y的简单氢化物的沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| CH3COOH | HC1O | H2CO3 |
| Ka=1.8×l0-5 | Ka=3.0×l0-8 | Ka1=4.4×l0-7Ka2=4.7×l0-11 |
| A. | 向NaClO溶液中通入少量CO2的离子方程式为:2C1O-+CO2+H2O═2HC1O+CO32- | |
| B. | 相同浓度的CH3COOH和NaClO的混合溶液中,水的电离程度前者大 | |
| C. | 向0.lmol•L-l的CH3COOH溶液中滴加NaOH溶液至pH=5,此时溶液的 c(CH3COOH):c(CH3COO-)=5:9 | |
| D. | 常温下,0•lmol•L-1 的 NaHC2O4 溶液 pH=4:c(HC2O4-)>c(H+)>c(H2C2O4)>c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com