
下列有关元素的性质及其递变规律正确的是
A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性从上到下依次减弱
D.同周期金属元素的化合价越高,其原子失电子能力越强
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
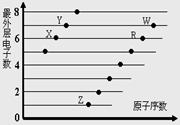
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是( )
A.ZY、ZW、W2X的水溶液都显酸性
B.原子半径大小:W>R>X, 简单离子半径大小:R >W >X
C.W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
D.Z与X,Z与R两种元素形成的化合物中均可能存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应水化物的酸性从左到右依次增强
D.第3周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学键的说法中错误的是( )
A.氯化钠熔化或氯化氢溶于水时都要破坏化学键
B.离子化合物中可能含有共价键,共价化合物中一定不含有离子键
C.氯化铵受热变成气体,冷却后又成晶体,此过程中化学键没有发生变化
D.碘晶体升华和冰融化时都未涉及化学键的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验现象得出的结论正确的是( )
| 选项 | 实验现象 | 结论 |
| A | 将BaSO4浸泡在饱和Na2CO3溶液中,部分BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| B | 某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成 | 该溶液中一定存在SO |
| C | 滴有酚酞的Na2CO3溶液中加入BaCl2固体,红色变浅 | Na2CO3溶液中存在水解平衡 |
| D | 溴水中通入SO2,溴水褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
B.用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度
C.邻苯二甲酸氢钾可用于标定NaOH溶液的浓度。假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小
D.向某溶液中加入茚三酮试剂,加热煮沸后溶液若出现蓝色,则可判断该溶液含有蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是一种综合处理SO2废气的工艺流程。下列说法正确的是( )
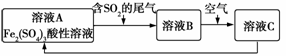
A.向B溶液中滴加KSCN溶液,溶液变为血红色
B.溶液B转化为溶液C发生的变化的离子方程式为4H++4Fe2++O2===4Fe3++2H2O
C.溶液酸性:A>B>C
D.加氧化亚铁可以使溶液C转化为溶液A
查看答案和解析>>
科目:高中化学 来源: 题型:
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是( )

|
| A. | 向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液中加入0.1 mol/L稀H2SO4溶液 |
|
| B. | 向含有0.1 mol/L AlCl3和0.3mol/L NH4Cl的1L混合液中加入0.1mol/L NaOH溶液 |
|
| C. | 向烧碱溶液中滴加明矾溶液 |
|
| D. | 向Ca(OH)2溶液中逐渐通入二氧化碳 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com