
| �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | ˮ���� | |
| ������ | 122.4 | 249 | 1.27 | �� |
| �״� | -97 | 64.3 | 0.79 | ���� |
| ��������� | -12.3 | 199.6 | 1.09 | ���� |
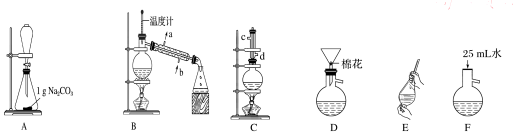
���� ��1�����Ũ�����ϡ�ͷ����������������Ƭ���Է�ֹ���У����������ӣ���Ҫֹͣ���ȣ���ȴ�����¼��룻
��2�����������������������ã������������������Һ���������������
��3����Բ����ƿ�м���0.1mol�������0.4mol�״�����С�ļ���3mLŨ���ᣬ���Ⱥ�Ͷ�뼸����ʯ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ�����з�Һ������Ȳ�����
��4����Ӧ��ȫ���б�����ʣ����Ҫͨ������Na2CO3��֮��Ӧ��ȥ�������̼���������л��������ù��˵ķ������룻
��5�����ݱ�����������ܶȼ���ȷ�ķ�Һ�����������н��
��� �⣺��1���ο�Ũ�����ϡ�ͣ��Ƚ�һ�����ı����������ƿ�У�Ȼ���ټ���״���������������һ������Ũ���������ƻ��Һ��
��ȱ�����Ƭ������������װ��C�������һ��ʱ��������ǼӴ�Ƭ��Ӧ��ֹͣ���ȣ���ȴ�ӣ�
�ʴ�Ϊ���Ƚ�һ�����ı����������ƿ�У�Ȼ���ټ���״���������������һ������Ũ�����ȴ�ӣ�
��2��Cװ���ϲ��������ܿ�ʹ��Ӧ��ϼ���ʱ�ӷ������������������»�����Ӧ�����У�����ԭ�ϵ���ģ���ȴˮ��ˮ�������������������෴��ѡ���d�ڽ��룬c��������
���������������Һ������������������Բ��ܻ�Ϊ���������ܣ�
�ʴ�Ϊ�������ռ���Ʒ����
��3����Բ����ƿ�м���0.1mol�������0.4mol�״�����С�ļ���3mLŨ���ᣬ���Ⱥ�Ͷ�뼸����ʯ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ������������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ�����з�Һ������Ȳ��������÷�Һ�ķ�����ȥ����������е����ᡢ�����ᣬȻ�������������˳��ΪCFEADB���ʴ�Ϊ��CFEADB��
��4��̼�����ܹ��뱽���ᷴӦ������̼����ϴȥ����������й���������������������ˮ��������̼�����ù��˵ķ����ɳ�ȥ��
�ʴ�Ϊ����ȥ����������еı������ȥû�з�Ӧ���Na2CO3��
��5�����ڱ�����������ܶȱ�ˮ���������ܣ����ˮ���ϲ㣬�����²㣬��Һʱ��ֱ�ӽ�����������ӷ�Һ©�����¿ڷų���������ȷ��Ϊb��
�ʴ�Ϊ��b��
���� ���⿼���Ʊ���������ƣ��漰���������Ĺ����밲װ�������ķ��롢�ᴿ�����ʵ���ȡ��ҩƷ��ѡ��ʹ�á����ʲ��ʵļ����֪ʶ����ȷʵ��Ŀ�ġ�ʵ��ԭ��Ϊ���ؼ�����Ŀ�ѶȽϴ����������ϴ�֪ʶ��϶࣬���������ѧ���ķ������������������Ӧ����ѧ֪ʶ��������


 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij����ԭ��ʾ��ͼ���£�������ǽ�ʳ��ˮ���ض������µ��õ��������ƣ�NaClO3�������ᷴӦ����ClO2��
ij����ԭ��ʾ��ͼ���£�������ǽ�ʳ��ˮ���ض������µ��õ��������ƣ�NaClO3�������ᷴӦ����ClO2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

| ��� | ����ɷ֣��ѧʽ�� |
| 1 | |
| 2 | |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �ܽ�ȣ�S��/g | �ܶȻ���Ksp�� | Ħ��������M��/g•mol-1 | |||
| Ca��OH��2 | Ba��OH��2 | CaCO3 | BaCO3 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9��10-9 | 2.6��10-9 | 100 | 197 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ࣨGe���ǵ��͵İ뵼��Ԫ�أ��ڵ��ӡ����ϵ�����Ӧ�ù㷺���ش��������⣺
�ࣨGe���ǵ��͵İ뵼��Ԫ�أ��ڵ��ӡ����ϵ�����Ӧ�ù㷺���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ������ | ȼ���� | ������ | ȼ���� |
| ���� | 891.0 | ������ | 2878.0 |
| ���� | 1560.8 | �춡�� | 2869.6 |
| ���� | 2221.5 | 2-������ | 3531.3 |
| A�� | �ȶ��ԣ������飾�춡�� | |
| B�� | ����ȼ�յ��Ȼ�ѧ����ʽΪ��2C2H6��g��+7O2��g���T4CO2��g��+6H2O��g����H=-1560.8KJ/mol | |
| C�� | �������ȼ���ȴ�Լ��3540 KJ/mol���� | |
| D�� | ��ͬ������������̼����������Խ����ȫȼ�շų�������Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
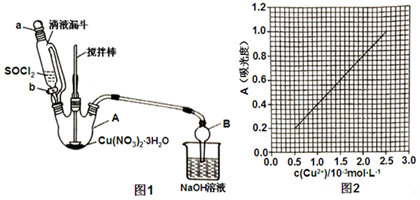
 ��֪��Һ�У���ԭ��HSO3-��I-��������IO3-��I2��SO42-���ں�3molNaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������
��֪��Һ�У���ԭ��HSO3-��I-��������IO3-��I2��SO42-���ں�3molNaHSO3����Һ����μ���KIO3��Һ�������KIO3��������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | a�㷴Ӧ�����ӷ���ʽΪ IO3-+3HSO3-=I-+3SO42-+3H+ | |
| B�� | b�㵽c�㷴Ӧ�����ӷ���ʽΪ IO3-+5I-+6H+=3I2+3H2O | |
| C�� | ����Һ�е�I-Ϊ0.4 molʱ�������KIO3ֻ��Ϊ0.4 mol | |
| D�� | ����100 mL 1mol/L��KIO3��Һ����εμ�NaHSO3��Һ����Ӧ��ʼʱ�����ӷ���ʽΪ 2IO3-+5HSO3-=I2+5SO42-+H2O+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com