
¹ŲÓŚĻĀĮŠø÷Ķ¼µÄŠšŹö£¬ÕżČ·µÄŹĒ

A£®¼×±ķŹ¾H2ÓėO2·¢Éś·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ŌņH2µÄČ¼ÉÕČČĪŖ483.6 kJ/mol
B£®ŅŅ±ķŹ¾ŗćĪĀŗćČŻĢõ¼žĻĀ·¢ÉśµÄæÉÄę·“Ó¦2NO2(g)  N2O4(g)ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬
N2O4(g)ÖŠ£¬ø÷ĪļÖŹµÄÅضČÓėĘäĻūŗÄĖŁĀŹÖ®¼äµÄ¹ŲĻµ£¬ĘäÖŠ½»µćA¶ŌÓ¦µÄדĢ¬ĪŖ»ÆŃ§Ę½ŗāדĢ¬
C£®±ū±ķŹ¾A”¢BĮ½ĪļÖŹµÄČܽā¶ČĖęĪĀ¶Č±ä»ÆĒéæö£¬½«A”¢B±„ŗĶČÜŅŗ·Ö±šÓÉt1 ÉżĪĀÖĮt2
ÉżĪĀÖĮt2 Ź±£¬ČÜÖŹµÄÖŹĮæ·ÖŹżB>A
Ź±£¬ČÜÖŹµÄÖŹĮæ·ÖŹżB>A
D£®¶”±ķŹ¾³£ĪĀĻĀ£¬Ļ”ŹĶHA”¢HBĮ½ÖÖĖįµÄĻ”ČÜŅŗŹ±£¬ČÜŅŗpHĖę¼ÓĖ®ĮæµÄ±ä»Æ£¬ŌņĶ¬ÅØ¶ČµÄNaAČÜŅŗµÄpHŠ”ÓŚNaBČÜŅŗ
D
½āĪöŹŌĢā·ÖĪö£ŗA”¢H2µÄČ¼ÉÕČČŹĒÖøÉś³ÉŅŗĢ¬Ė®Ź±·Å³öµÄČČĮ棬A“ķĪó£»B”¢Ę½ŗāŹ±ÓĆNO2ŗĶN2O4±ķŹ¾µÄ·“Ó¦ĖŁĀŹÓ¦ĪŖ2£ŗ1µÄ¹ŲĻµ£¬B“ķĪó£»C”¢ÓÉt1 ÉżĪĀÖĮt2
ÉżĪĀÖĮt2 Ź±£¬ČÜÖŹµÄÖŹĮæ·ÖŹżĻąµČ£¬C“ķĪó£»DÕżČ·£¬Ėį»ņ¼īĻ”ŹĶĻąĶ¬±¶ŹżĖįŠŌ»ņ¼īŠŌĒæµÄpH±ä»Æ·¶Ī§“ó”£
Ź±£¬ČÜÖŹµÄÖŹĮæ·ÖŹżĻąµČ£¬C“ķĪó£»DÕżČ·£¬Ėį»ņ¼īĻ”ŹĶĻąĶ¬±¶ŹżĖįŠŌ»ņ¼īŠŌĒæµÄpH±ä»Æ·¶Ī§“ó”£
æ¼µć£ŗ漲鷓ӦČČ”¢»ÆŃ§Ę½ŗāדĢ¬µÄÅŠ¶Ļ”¢Čܽā¶ČĒśĻß”¢Čõµē½āÖŹµÄĻ”ŹĶµČĻą¹ŲÖŖŹ¶”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠÓŠ¹ŲČČ»Æѧ·½³ĢŹ½µÄŠšŹöÕżČ·µÄŹĒ
| A£®2H2(g)£«O2(g)===2H2O(g)£»”÷H=£483£®6 kJ/mol£¬ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241£®8 kJ |
| B£®ŅŃÖŖC(ŹÆÄ«£¬s)="==" C(½šøÕŹÆ£¬s) ”÷H£¾0£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø |
| C£®ŗ¬20£®0g NaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28£®7 kJµÄČČĮ棬ŌņøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗNaOH(aq)£«HCl(aq)===NaCl(aq)£«H2O(l)£»”÷H=£57£®4 kJ/mol |
| D£®ŅŃÖŖ2C(s)£«2O2(g)==2CO2(g)£»”÷H1 £»2C(s)£«O2(g)="2CO(g)" ”÷H2”£Ōņ”÷H1£¾”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ£ŗH(g) + H(g) £½ H2(g) ¦¤H£½£435.7kJ/mol£¬“ĖČČ»Æѧ·½³ĢŹ½°üŗ¬µÄŅāŅåŹĒ
| A£®ĒāŌ×ÓµÄÄÜĮæ±ČĒā·Ö×ÓµÄÄÜĮæµĶ |
| B£®Į½øöĒāŌ×Ó½įŗĻ³ÉŅ»øöĒā·Ö×ÓŹ±·Å³ö435.7kJÄÜĮæ |
| C£®1molĒā·Ö×Ó·Ö½ā³É2molĒāŌ×ÓŅŖĪüŹÕ435.7kJÄÜĮæ |
| D£®2molĒāŌ×Ó½įŗĻ1molĒā·Ö×Ó³ÉŅŖĪüŹÕ435.7kJÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¹ż³ĢÖŠ¦¤HŠ”ÓŚĮćµÄŹĒ
| A£®ĀČĖį¼Ų·Ö½āÖĘŃõĘų |
| B£®ĀČ»Æļ§ŹÜČČ·Ö½ā |
| C£®ĒāĘų»¹ŌŃõ»ÆĶ |
| D£®ŹµŃéŹŅÓĆŠæŗĶĻ”ĮņĖį·“Ó¦ÖĘĒāĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»ÆŹĒÓÉ»Æѧ·“Ó¦ÖŠ¾É»Æѧ¼ü¶ĻĮŃŹ±ĪüŹÕµÄÄÜĮæÓėŠĀ»Æѧ¼üŠĪ³ÉŹ±·Å³öµÄÄÜĮæ²»Ķ¬ŅżĘšµÄ”£ČēĻĀĶ¼ĪŖN2(g)ŗĶO2(g)·“Ӧɜ³ÉNO(g)¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
| A£®1 mol N2(g)ŗĶ1 mol O2(g)·“Ó¦·Å³öµÄÄÜĮæĪŖ180 kJ |
| B£®1 mol N2(g)ŗĶ1 mol O2(g)¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2 mol NO(g)¾ßÓŠµÄ×ÜÄÜĮæ |
| C£®Ķس£ĒéæöĻĀ£¬N2(g)ŗĶO2(g)»ģŗĻÄÜÖ±½ÓÉś³ÉNO |
| D£®NOŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
¼üÄÜŹĒÖøĘĘ»µ£Ø»ņŠĪ³É£©1mol»Æѧ¼üĖłĪüŹÕ£Ø»ņ·Å³ö£©µÄÄÜĮ攣ĻÖ²éµĆ£ŗH£H”¢Cl£ClŗĶH£ClµÄ¼üÄÜ·Ö±šĪŖ436kJ/mol”¢243kJ/molŗĶ431kJ/mol£¬ĒėÓĆ“ĖŹż¾Ż¹Ą¼Ę£¬ÓÉCl2”¢H2Éś³É1molHClŹ±µÄČČŠ§Ó¦ĪŖ£Ø £©
| A£®·ÅČČ91£®5kJ | B£®·ÅČČ183kJ | C£®ĪüČČ183kJ | D£®ĪüČČ91£®5kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
Ėį¼īÖŠŗĶ·“Ó¦ NaOH£Ø?£©+ HCl£Ø?£©”śNaCl£Ø?£©+ H2O(?)+57.6 kJÖŠ,ĪŹŗűķŹ¾µÄדĢ¬ÕżČ·µÄŹĒ
| A£®NaOH£ŗ¹Ģ | B£®ŃĪĖį£ŗŅŗ | C£®NaCl£ŗČÜŅŗ | D£®H2O£ŗČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ£ŗC(s)£«H2O(g)£½CO(g)£«H2(g) ”÷H£½a kJ/mol
C(s)£«O2(g)£½2CO(g) ”÷H£½£220 kJ/mol
H£H”¢O£½OŗĶO£H¼üµÄ¼üÄÜ·Ö±šĪŖ436”¢496ŗĶ462 kJ/mol£¬ŌņaĪŖ
| A£®£332 | B£®£118 | C£®£«350 | D£®£«130 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĀČŌ×Ó¶ŌO3µÄ·Ö½āÓŠ“ß»Æ×÷ÓĆ£ŗO3£«Cl£½ClO£«O2””¦¤H1£¬ClO£«O£½Cl£«O2””¦¤H2”£“óĘų³ōŃõ²ćµÄ·Ö½ā·“Ó¦ŹĒ£ŗO3£«O£½2O2””¦¤H£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠŠšŹöÕżČ·µÄŹĒ(””””)”£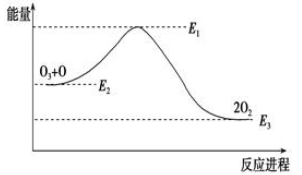
¢Ł·“Ó¦O3£«O£½2O2µÄ¦¤H£½E1£E3””¢Ś·“Ó¦O3£«O£½2O2ŹĒ·ÅČČ·“Ó¦””¢Ū¦¤H£½¦¤H1£«¦¤H2””¢Ü“óĘų²ćÖŠµÄ³ōŃõĪŽ·ØŌŁÉś
| A£®¢Ł¢Ś | B£®¢Ś¢Ū | C£®¢Ū¢Ü | D£®¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com